
| A. | 二氧化硫可用于抑制酒类中细菌生长,可在葡萄酒中微量添加 | |
| B. | 二氧化硫能使品红褪色,加热后颜色不能恢复 | |
| C. | 二氧化硫使酸性高锰酸钾褪色,体现了二氧化硫的漂白性 | |
| D. | 二氧化硫属于碱性氧化物,可以用NaOH溶液吸收 |
分析 A.二氧化硫具有还原性,可抑制酒类中细菌生长;
B.二氧化硫的漂白为暂时性漂白;
C.二氧化硫与高锰酸钾发生氧化还原反应;
D.二氧化硫为酸性氧化物.
解答 解:A.二氧化硫具有还原性,可抑制酒类中细菌生长,则在葡萄酒中微量添加,故A正确;
B.二氧化硫的漂白为暂时性漂白,则使品红褪色后,加热后颜色恢复为红色,故B错误;
C.二氧化硫与高锰酸钾发生氧化还原反应,高锰酸钾褪色,体现了二氧化硫的还原性,故C错误;
D.二氧化硫为酸性氧化物,有毒,与碱反应生成盐和水,则用NaOH溶液吸收,故D错误;
故选A.
点评 本题考查二氧化硫的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=3的H2SO4和pH=11的氨水 | |
| B. | 0.1 mol/L的盐酸和0.2 mol/L的醋酸钠溶液 | |
| C. | 等物质的量浓度的盐酸和氨水 | |
| D. | 等物质的量浓度的硫酸和NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).
某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).
 ,该反应的类型为酯化反应或取代反应.
,该反应的类型为酯化反应或取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
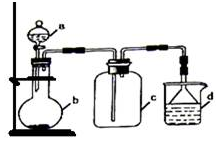 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略了净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略了净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度 | |
| B. | 保持容器的体积不变,增加A(g)的物质的量 | |
| C. | 保持容器的压强不变,充入氦气 | |
| D. | 保持容器的体积不变,充入氦气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 装 置 | 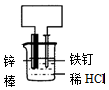 |  |  |  |
| 结论 | 能防止铁钉腐蚀 | 能证明非金属性Cl>C>Si | 能分离出Cl2与KI溶液反应生成的碘 | 可制取乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铁溶液常用于腐蚀铜制印刷电路板 | |
| B. | 钢铁锈蚀后可以避免再锈蚀 | |
| C. | 明矾可用于净水 | |
| D. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com