
已知下列物质都能氧化H2S,它们氧化H2S时自身分别发生下列变化:Fe3+→Fe2+;Cr2O72?→2Cr3+;Br2→2Br-;HNO3→NO.如果氧化等物质的量的H2S气体得到S单质,需要上述离子或物质的物质的量最小的是
A.Fe3+ B.Br2 C.Cr2O72? D.HNO3
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源:2015-2016学年浙江省高一上期中测试化学试卷(解析版) 题型:选择题
同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是
A.3Br2+6KOH=5KBr+KBrO3+3H2O B.MnO2+4HCl(浓)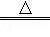 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.2KNO3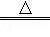 2KNO2+O2↑ D.NH4NO3
2KNO2+O2↑ D.NH4NO3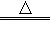 N2O↑+2H2O
N2O↑+2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:填空题
反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
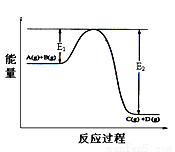
(1)该反应是_________反应(填“吸热”或“放热”);
反应热△H=_______;(用E1、E2表示)
(2)反应体系中加入催化剂对反应热是否有影响? _________,原因是_______________;
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化
是:E1_______,E2_______(填 “增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上第二次质检化学试卷(解析版) 题型:选择题
据所载我国最近合成新的同位素,其中一种是 (铪),它的质子数是
(铪),它的质子数是
A.72 B.113 C.185 D.257
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古赤峰二中高二上第二次月考化学试卷(解析版) 题型:选择题
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:下列有关叙述正确的是

A.贝诺酯分子中有三种含氧官能团
B.用FeCl3 溶液不能区别乙酰水杨酸和对乙酰氨基酚
C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3 溶液反应
D. 1mol贝诺酯与足量NaOH 溶液共热最多可消耗5molNaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:实验题
三氯化碘(ICl3,I的化合价为+3价)在药物合成中用途广泛,其熔点:33℃,沸点:73℃,实验室可用如图装置制取ICl3。

(1)制备氯气选用的药品为漂白精固体(主要成分为Ca(ClO)2)和浓盐酸,相关反应的化学方程式为:____________________________;
试剂X为________________、Y为______________;
(2)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C中是否发生堵塞,请写出发生堵塞时B中的现象____________________________;
(3)某同学欲测定ICl3样品中ICl3的纯度,他准确称取ICl3样品10.0g于烧杯中,加入适量水和过量KI晶体,充分反应:ICl3+3KI═2I2+3KCl(样品中杂质不反应).将所得溶液配置成100mL待测液.取25.00mL待测液,用2.0mol/L的Na2S2O3标准液滴定(I2+2S2O32-═2I-+S4O62-),以淀粉溶液作指示剂,达到终点时的现象为____________________________;重复滴定,实验数据记录如下:
滴定次数 | 待测液体积/mL | Na2S2O3标准液体积/mL | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
第三次 | 25.00 | 4.20 | 26.70 |
该样品中ICl3的质量分数为_______________(ICl3相对分子质量为233.5)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏山南第二高级中学高一上期末化学试卷(解析版) 题型:选择题
下列各选项的每组两种物质在溶液中反应,可用同一离子方程式表示的是
A.氢氧化钠与盐酸;氢氧化铜与盐酸
B.BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液
C.Na2CO3溶液与硝酸溶液;CaCO3与硝酸溶液
D.石灰石与硝酸反应;石灰石与盐酸
查看答案和解析>>
科目:高中化学 来源:2016届贵州市高三上学期第五次月考理综化学试卷(解析版) 题型:实验题
纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。
(1)工业上二氧化钛的制备方法是:
Ⅰ.将干燥后的金红石(主要成分是TiO2,主要杂质是SiO2)与碳粉混合放入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4.
Ⅱ.将SiCl4分离,得到纯净的TiCl4.
Ⅲ.向TiCl4中加水,加热,水解得到沉淀TiO2•xH2O.
Ⅳ.将TiO2•xH2O高温分解得到TiO2.
资料卡片 | ||
物质 | 熔点 | 沸点 |
SiCl4 | -70℃ | 57.6℃ |
TiCl4 | -25℃ | 136.5℃ |
①据资料卡片中信息判断,TiCl4与SiCl4在常温下的状态是_____;分离二者所采取的操作名称是____。
②Ⅲ中反应的化学方程式是________。
③如在实验室中完成步骤IV,应将TiO2•xH2O放在_____(填字母序号图 1)中加热。
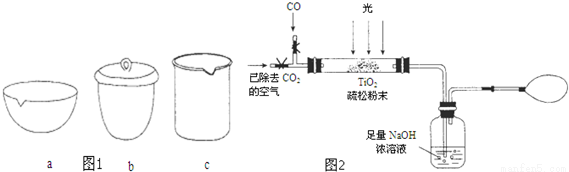
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或 水中的氧获得,生成H2O2.H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的__________(填“氧化性”或“还原性”)。
(3)图2是某研究小组用下列装置模拟“生态马路”的部分原理(夹持装置已略去).
①缓慢通入22.4L(已折算成标准状况)CO气体和足量空气,最终测得NaOH溶液增重11g,则CO 的转化率为________。
②实验①中,当CO气体全部通入后,还要再通一会儿空气,其目的是________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上期中测试化学试卷(解析版) 题型:选择题
在一个恒温、恒容密闭容器中,有两个可左右自由滑动的密封隔板(a、b),将容器分成三部分,已知充入的三种气体质量相等,当隔板静止时,容器内气体所占体积如图所示( ),下列说法中错误的是( )

A.若Y是C4H8,则X可能是N2
B.分子数目:X=Z=2Y
C.若X是O2,则Z不可能是CO2
D.气体密度:X=Z=2Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com