
| A、①③④ | B、③④⑤ |
| C、②③④ | D、①②⑤ |


科目:高中化学 来源: 题型:
35 17 |
37 17 |
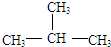 E、
E、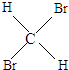 与
与
查看答案和解析>>
科目:高中化学 来源: 题型:
209 84 |
209 84 |
| A、质子数是125 |
| B、中子数是84 |
| C、质量数是209 |
| D、核外电子数125 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a>b>c |
| B、a>c>b |
| C、c>b>a |
| D、b>c>a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg和Ag |
| B、Al和Zn |
| C、Al和Fe |
| D、Mg和Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在FeCl3溶液中投入足量的Zn粉:2Fe3++Zn═Zn2++2Fe2+ |
| B、NaHSO4溶液与Ba(OH)2溶液混合后呈中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
| C、磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
| D、Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Si 和H2SO4 |
| B、Na和MgCl2 |
| C、CaC2和CuSO4 |
| D、Na2O和NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com