
| Z | |
| X | Y |
| A. | Z元素的最高化合价一定大于X元素 | |
| B. | 三种元素原子半径由高到低的顺序一定是Y>X>Z | |
| C. | 若它们的原子最外层电子数之和为11,则X为金属元素 | |
| D. | 若它们均为金属元素,则Y的最高价氧化物对应水化物的碱性最强 |
分析 由短周期元素在周期表中的位置可知,Z处于第二周期,X、Y处于第三周期,
A.若Z处于ⅥA族或ⅦA族时,Z元素一般没有最高正化合价;
B.同周期元素从左到右原子半径逐渐减小;
C.若它们的原子最外层电子数之和为11,令X最外层电子数为a,Y、Z最外层电子数为a+1,则a+a+1+a+1=11,解得a=3,故X为Al、Y为Si、Z为C;
D.若它们均为金属元素,则X为Na、Y为Mg、Z为Be.
解答 解:由短周期元素在周期表中的位置可知,Z处于第二周期,X、Y处于第三周期,
A.若Z处于ⅥA族或ⅦA族时,为O或F元素,最高正化合价,故A错误;
B.同周期元素从左到右原子半径逐渐减小,应为X>Y,故B错误;
C.若它们的原子最外层电子数之和为11,令X最外层电子数为a,Y、Z最外层电子数为a+1,则a+a+1+a+1=11,解得a=3,故X为Al、Y为Si、Z为C,故C正确;
D.若它们均为金属元素,则X为Na、Y为Mg、Z为Be,X的最高价氧化物对应水化物的碱性最强,故D错误.
故选C.
点评 本题考查结构性质位置关系、元素周期律等,难度不大,注意掌握周期表中的特殊性,利用列举法解答,注意对元素周期表的整体把握,注意对元素周期律的理解掌握.


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:选择题
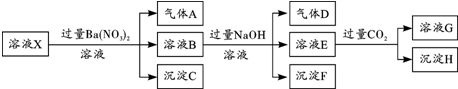
| A. | 沉淀H为Al(OH)3、BaCO3的混合物 | |
| B. | 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl- | |
| C. | 溶液X中一定含有Al3+、NH4+、Fe2+、SO42-、H+ | |
| D. | 若溶液X为100 mL,产生的气体A为44.8 mL(标况),则X中c(Fe2+)=0.06 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、H2SO4、(NH4)2SO4 | B. | MgO、Na2SO4、NH4HCO3 | ||
| C. | Na2O2、NH4Cl、Na2SO4 | D. | HCl、Al2O3、MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
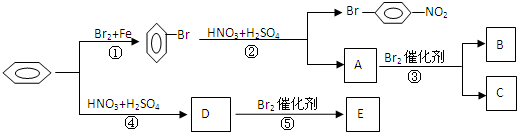
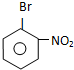 B
B 或
或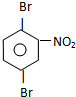 C
C 或
或 D
D E
E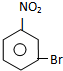
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
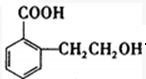
 乙基香兰素是一种合成香料,其结构简式如图:
乙基香兰素是一种合成香料,其结构简式如图: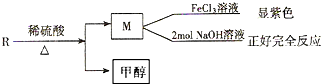
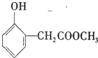 、
、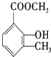 ;
;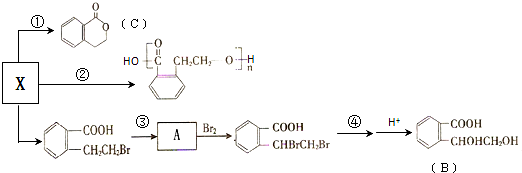
 ;B中含氧官能团的名称羟基、羧基;
;B中含氧官能团的名称羟基、羧基; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和镁分别与冷水反应,判断钠和镁金属性强弱 | |
| B. | Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱 | |
| C. | 硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱 | |
| D. | 在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
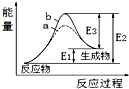
| A. | 该反应为放热反应 | |
| B. | b表示的有催化剂 | |
| C. | 催化剂能降低正、逆反应的活化能 | |
| D. | 逆反应的活化能大于正反应的活化能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com