
| 阳离子 | 阴离子 |
| Na+ Ca2+ Fe 2+ Al3+ Fe 3+ Mg3+ | OH- HCO3- CO32- Cl- NO3- SO42- |
| A. | X溶液中不可能含有HCO3-或CO32- | |
| B. | 生成无色气体的离子方程式为:3Fe2++NO3-+4H+═3Fe3++NO+2H2O | |
| C. | 根据电荷守恒,原溶液中一定含Mg2+ | |
| D. | X溶液中一定含3种阳离子、2种阴离子 |
分析 各种离子的物质的量浓度均为0.1mol/L,向溶液X中加入足量的盐酸,有气体生成,且反应溶液中阴离子的种类没有变化,产生气体不可能是碳酸根离子或碳酸氢根离子;根据表中的离子,可以推知是Fe2+、NO3-在酸性环境下生成的一氧化氮,加入盐酸,溶液中阴离子种类不变,所以原来溶液中含有Cl-,若只含有氯离子和硝酸根离子,二者的浓度为0.1mol/L,根据电荷守恒是不可能的,所以还含有阴离子SO42-,由于总共含有5种离子,再根据电荷守恒可知还含有一种带有两个正电荷的Mg2+,所以原溶液中含有的五种离子为:Cl-、NO3-、SO42-、Fe2+、Mg2+,据此进行解答.
解答 解:各种离子的物质的量浓度均为0.1mol/L,向溶液X中加入足量的盐酸,有气体生成,且反应溶液中阴离子的种类没有变化,产生气体不可能是碳酸根离子或碳酸氢根离子;根据表中的离子,可推知是Fe2+、NO3-在酸性环境下生成的一氧化氮,加入盐酸,溶液中阴离子种类不变,所以原来溶液中含有Cl-,若只含有氯离子和硝酸根离子,二者的浓度为0.1mol/L,根据电荷守恒是不可能的,所以还含有阴离子SO42-,由于总共含有5种离子,再根据电荷守恒可知还含有一种带有两个正电荷的Mg2+,所以原溶液中含有的五种离子为:Cl-、NO3-、SO42-、Fe2+、Mg2+,
A.根据分析可知,溶液中一定不存在HCO3-与CO32-,故A正确;
B.生成无色气体为NO,反应的离子方程式为:3Fe2++NO3-+4H+═3Fe3++NO+2H2O,故B正确;
C.原溶液中一定含有Mg2+,故C正确;
D.原溶液中含有的五种离子为:Cl-、NO3-、SO42-、Fe2+、Mg2+,含有2种阳离子、3种阴离子,故D错误;
故选D.
点评 本题考查了常见离子的检验方法,题目难度中等,明确常见离子的性质为解答关键,注意熟练掌握常见离子的性质,能够根据电荷守恒判断离子的存在情况,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
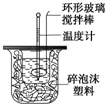 利用下图装置测定中和热的实验步骤如下:
利用下图装置测定中和热的实验步骤如下:| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ②③⑤ | C. | ④⑤ | D. | ②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
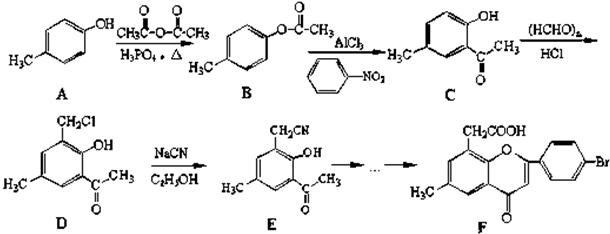
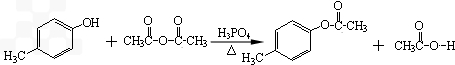 .
.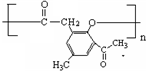 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.3mol/L | D. | 0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 往Fe(OH)3胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解 | |
| C. | 纳米材料粒子直径一般从几纳米到几十纳米,因此纳米材料属于胶体 | |
| D. | 水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘粒子带电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 学生甲 | 学生乙 |
| A | 向NaHCO3溶液中逐滴加入盐酸 | 向盐酸中逐滴加入NaHCO3溶液 |
| B | 向AlCl3溶液中滴加NaOH溶液 | 向NaOH溶液中滴加入AlCl3溶液 |
| C | 向FeCl2溶液中滴加KSCN溶液,再通入Cl2 | 向FeCl2溶液中通入Cl2,再滴加KSCN溶液 |
| D | 向Al2(SO4)3溶液中滴加氨水 | 向Al2(SO4)3溶液中滴加NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去硬脂酸钠溶液中的甘油方法是:往溶液中加入饱和食盐水,分液 | |
| B. | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去,证明生成的气体全部是乙烯 | |
| C. | 润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从下口倒出,重复2~3次 | |
| D. | 取5mL0.1mol•L-1KI溶液,滴加0.1mol•L-1FeCl3溶液5~6滴,继续加入2mLCCl4,充分振荡后静置,取上层溶液加KSCN溶液,无明显现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com