
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源:2015-2016学年山西晋城市高二下期中理科化学卷(解析版) 题型:选择题
要证明某溶液中不含Fe3+而可能含有Fe2+.进行如下实验操作时最佳顺序为( )
①加入适量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液.
A.①③ B.③② C.③① D.①②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海省高一下期末化学试卷(解析版) 题型:选择题
元素X的原子有3个电子层,最外层有4个电子.这种元素位于周期表的( )
A. 第4周期ⅢA族 B. 第4周期ⅦA族 C. 第3周期Ⅳ族 D. 第3周期ⅣA族
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省高三上学期第一次质检化学试卷(解析版) 题型:选择题
如图,相同条件下,两个容积相同的试管分别装满NO2和NO气体,分别倒置于水槽中,然后通过导管缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内充满液体。假设试管内的溶质不向水槽中扩散,则两个试管内溶液物质的量浓度之比为
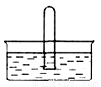
A.5∶7 B. 1∶1 C.7∶5 D.4∶3
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省高三上学期第一次质检化学试卷(解析版) 题型:选择题
根据下图海水综合利用的工业流程图,判断下列说法正确的是( )
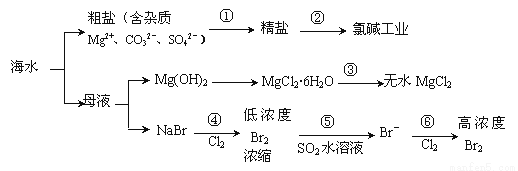
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B.除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
C.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
D.在过程④、⑥反应中每氧化0.2 mol Br-需消耗0.1mol Cl2
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第二次周测化学试卷(解析版) 题型:实验题
高铁酸钾是绿色、环保型水处理剂,也是高能电池的电极材料。工业上,利用硫酸亚铁为原料,通过铁黄(FeOOH)制备高铁酸钾,可降低生产成本且产品质量优。工艺流程如下:
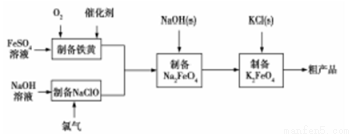
回答下列问题:
(1)有同学认为上述流程可以与氯碱工业联合。写出电解饱和食盐水制取次氯酸钠的化学方程式 。
(2)制备铁黄的反应中氧化剂与还原剂的物质的量之比为 。实验测得反应溶液的pH、温度对铁黄产率的影响如图所示。反应温度宜选择 ;pH大于4.5时铁黄产率降低的主要原因可能是 。
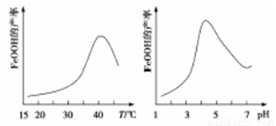
(3)用高铁酸钾处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3、CN-等,生成的氢氧化铁胶体粒子还能吸附水中悬浮杂质。试写出高铁酸钾处理含CN-废水时除去CN-的离子方程式 。
(4)K2FeO4可作锌铁碱性高能电池的正极材料,电池反应原理:
2K2FeO4+3Zn+8H2O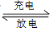 2Fe(OH)3+3Zn(OH)2+4KOH。放电时负极材料是 ;充电时阳极的电极反应式为 。
2Fe(OH)3+3Zn(OH)2+4KOH。放电时负极材料是 ;充电时阳极的电极反应式为 。
(5)已知:常温下,Kap[Fe(OH)3]=4.0×10-38。高铁酸钾的净水能力与废水的pH有关,当溶液pH=2时,废水中c(Fe3+)= mol·L-1。
(6)如果上述流程中,铁元素总利用率为75%。利用1mol 2mol·L-1FeSO4溶液能制备纯度为90%的高铁酸钾 kg。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第二次周测化学试卷(解析版) 题型:选择题
下列实验,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 在含酚酞的碳酸钠溶液中滴加氯化钙溶液 | 生成白色沉淀,溶液颜色无明显变化 | 生成了碳酸钙,不影响盐类水解 |
B | 常温下,测定不同浓度的硫酸铵溶液pH | 浓度较大的pH较小 | 浓度越大,同条件下盐水解程度越大 |
C | 在同浓度的盐酸中分别加入等量的锌粒和锌粉 | 加入锌粉的试管产生气泡速度较快 | 其他条件相同,固体接触面积越大,化学反应速率越大 |
D | 在含氢氧化镁和氢氧化钠的浊液中滴加氯化铁溶液 | 白色沉淀转化成红褐色沉淀 | 氢氧化铁的溶度积小于氢氧化镁的溶度积 |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第一次月考理综化学试卷(解析版) 题型:推断题
现有某混合物的无色透明溶液,可能含有以下离子中的若干种:
Na+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各100mL溶液进行如下实验:
①第一份加入足量AgNO3溶液有沉淀产生,加足量稀硝酸后沉淀部分溶解;
②第二份加足量NaOH溶液充分加热后,收集到气体0.896L(标准状况);
③第三份加足量BaCl2溶液后,过滤后充分干燥得到沉淀6.27g,再经足量稀硝酸洗涤、干燥后,沉淀质量变为2.33g。根据上述实验现象和有关数据,回答下列问题:
(1)原溶液中一定存在的阴离子是 ,一定不存在的离子是 ,可能存在的离子是 。
(2)②中发生化学反应的离子方程式为 。
(3)③中生成可溶于稀硝酸的沉淀化学式为 ,物质的量为 mol,该沉淀溶于稀硝酸的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2017届河南信阳高考化学暑假自学自测专练:原子结构与性质(解析版) 题型:简答题
已知A原子只有一个未成对电子,M电子层比N电子层多11个电子,试回答下列问题:
(1)N电子层的s轨道和p轨道中只有一个未成对电子的元素有哪些?
(2)写出A原子的电子排布式和元素符号。
(3)指出元素A在周期表中的位置。
(4)指出元素A的最高化合价和最低化合价。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com