
| A. | 食物腐败 | B. | 植物光合作用 | C. | 金属生锈 | D. | 石膏点制豆腐 |
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应中PdCl2作氧化剂,被还原 | B. | 每转移2 mol e-时,生成1 mol X | ||
| C. | 未知物质X为CO2,属于还原产物 | D. | 还原性:CO>Pd |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
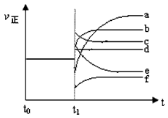 按要求回答下列问题:
按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
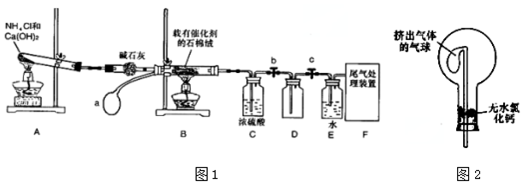
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠燃烧产生火灾时,不能用水来灭火 | |
| B. | 把钠保存在石蜡油或煤油中,以隔绝空气 | |
| C. | 钠投入硫酸铜溶液中,剧烈反应后能生成金属铜 | |
| D. | 向滴有酚酞的蒸馏水中加入绿豆大小的一块钠,可观察到溶液变红的现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 已知2SO2(g)+O2(g)?2SO3(g)△H=-196.64kJ•mol-1,在容器中充入1mol SO2和0.5mol O2充分反应,放出的热量为98.32KJ | |
| C. | 已知在120C、101kPa时,1gH2燃烧生成水蒸气放出121KJ,其热化学方程式表示为H2(g)+$\frac{1}{2}$O2(g)=2H2O(l)△H=-242KJ/mol | |
| D. | CO(g) 的燃烧热是283.0kJ•mol-1,则CO2(g)=CO(g)+$\frac{1}{2}$O2(g)△H=+283kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9:6:0 | B. | 4:3:1 | C. | 3:3:2 | D. | 7:6:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com