
| A. | 盐酸 | B. | CuSO4溶液 | C. | NaOH溶液 | D. | H2O |
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:填空题
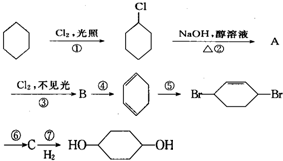 从环己烷可制备1,4-环己二醇,下列有关7步反应(其中无机产物都已略去),其中有2步属于取代反应,2步属于消去反应,3步属于加成反应.试回答:
从环己烷可制备1,4-环己二醇,下列有关7步反应(其中无机产物都已略去),其中有2步属于取代反应,2步属于消去反应,3步属于加成反应.试回答: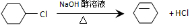 ;
; .
. ,C
,C .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 1:3 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa与足量氧气充分反应转移电子数目为NA | |
| B. | 1L0.1mol/LHCl溶液中含0.1NAHCl分子 | |
| C. | 100ml 1mol/L盐酸与0.1molNa2CO3无论如何滴加都产生0.05NA的CO2分子 | |
| D. | 0.1mol/L的AlCl3中Cl-的物质的量为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
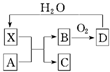 已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )| A. | X使蔗糖变黑的现象主要体现了X的强氧化性 | |
| B. | 若A为铁,则足量A与X在室温下即可完全反应 | |
| C. | 若A为碳单质,则将C通入少量的澄清石灰水中,最后有白色沉淀产生 | |
| D. | 工业上,B转化为D的反应条件为加热、使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4L 0.5 mol/L NaCl 溶液 | B. | 1L 0.3 mol/L Na2SO4 溶液 | ||
| C. | 0.8L 0.4 mol/L NaOH 溶液 | D. | 2L 0.15 mol/L Na3PO4 溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com