
(16分)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛 应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
(1)该反应的化学方程式为 ▲ ,每生成1molNF3,转移的电子数为 ▲ ,生成物NF3中氮原子的杂化方式为 ▲ ,NF3分子空间构型为 ▲ ;
▲ ,生成物NF3中氮原子的杂化方式为 ▲ ,NF3分子空间构型为 ▲ ;
(2)N、F两种元素的氢化物稳定性比 较,NH3 ▲ HF(
较,NH3 ▲ HF( 选填“>”或“<”);
选填“>”或“<”);
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式 ▲ ;
(4) 氯化铜溶液中加入过量氨水,可以生成四氨合铜络离子, 写出该反应的化学方程式 ▲ ;
(5)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如左图,该离子化合物的化学式为 ▲ 。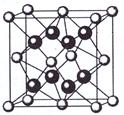
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源:2011-2012学年江苏省南通市高三上学期期中考试化学试卷 题型:填空题
(16分)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
(1)该反应的化学方程式为 ▲ ,每生成1molNF3,转移的电子数为 ▲ ,生成物NF3中氮原子的杂化方式为 ▲ ,NF3分子空间构型为 ▲ ;
(2)N、F两种元素的氢化物稳定性比较,NH3 ▲ HF(选填“>”或“<”);
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式 ▲ ;
(4) 氯化铜溶液中加入过量氨水,可以生成四氨合铜络离子, 写出该反应的化学方程式 ▲ ;
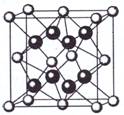
(5)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如左图,该离子化合物的化学式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山西省高三10月份月考化学试卷 题型:填空题
(16分)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
(1)该反应的化学方程式为 ,每生成1molNF3,转移的电子数为
生成物NF3中氮原子的杂化方式为 ,NF3分子空间构型为 ;
(2)N、F两种元素的氢化物稳定性比较,NH3 HF(选填“>”或“<”);
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式 ;
(4)氯化铜溶液中加入过量氨水,可以生成四氨合铜络离子, 写出该反应的化学方程式 ;
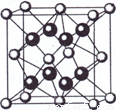
(5)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如左图,该离子化合物的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
(1)该反应的化学方程式为 ,每生成1molNF3,转移的电子数为
生成物NF3中氮原子的杂化方式为 ,NF3分子空间构型为 ;
(2)N、F两种元素的氢化物稳定性比较,NH3 HF(选填“>”或“<”);
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式 ;
(4)氯化铜溶液中加入过量氨水,可以生成四氨合铜络离子, 写出该反应的化学方程式 ;
(5)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如左图,该离子化合物的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2012届山西省太原五中高三10月份月考化学试卷 题型:填空题
(16分)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛 应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
(1)该反应的化学方程式为 ,每生成1molNF3,转移的电子数为 
生成物NF3中氮原子的杂化方式为 ,NF3分子空间构型为 ;
(2)N、F两种元素的氢化物稳定性比 较,NH3 HF(选填“>”或“<”);
较,NH3 HF(选填“>”或“<”);
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式 ;
(4)氯化铜溶液中加入过量氨水,可以生成四氨合铜络离子,写出该反应的化学方程式 ;
(5)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如左图,该离子化合物的化学式为 。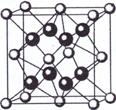
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com