
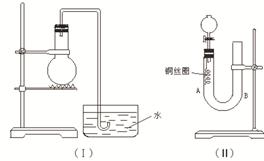


科目:高中化学 来源:不详 题型:单选题
| A.该反应是分解反应 |
| B.该反应是放热反应 |
| C.该反应生成物的化学式为 Fe2S3 |
| D.生成物硫化亚铁的总能量高于反应物铁粉和硫粉的总能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.2mL | B.2.4mL | C.3.6mL | D.3mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜片 | B.银片 | C.铁片 | D.锌片 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
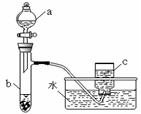
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.液氨作为清洁能源的反应原理是4NH3+5O2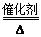 4NO+6H2O 4NO+6H2O |
| B.液氨具有腐蚀性和毒性,在使用过程中要防止液氨泄漏 |
| C.氨气比空气轻,标准状况下密度约为0.76 g·L-1 |
| D.氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
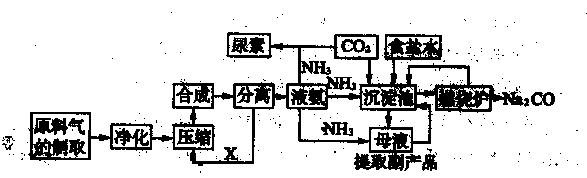
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com