
下列曲线图(纵坐标为沉淀的量,横坐标为加入物质的量)与对应的选项相符合的是( )
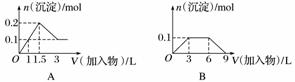
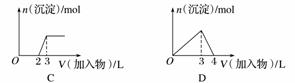
A.向1 L浓度均为0.1 mol·L-1的Ba(OH)2、NaAlO2混合溶液中加入0.1 mol·L-1的稀H2SO4
B.向1 L浓度分别为0.1 mol·L-1和0.3 mol·L-1的AlCl3、NH4Cl的混合溶液中加入0.1 mol·L-1的稀NaOH溶液
C.向烧碱溶液中滴加明矾溶液
D.向AlCl3溶液中滴加过量氨水
答案 A
解析 A项,Ba(OH)2和NaAlO2中加入H2SO4,发生的反应依次为Ba2++2OH-+2H++SO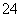 ===BaSO4↓+2H2O、AlO
===BaSO4↓+2H2O、AlO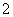 +H++H2O===Al(OH)3↓、Al(OH)3+3H+===Al3++3H2O,所以加1 L H2SO4时,Ba(OH)2反应完,再加0.5 L H2SO4时AlO
+H++H2O===Al(OH)3↓、Al(OH)3+3H+===Al3++3H2O,所以加1 L H2SO4时,Ba(OH)2反应完,再加0.5 L H2SO4时AlO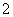 参加反应,再加1.5 L H2SO4时,Al(OH)3全部溶解,A正确;B项,向1 L浓度分别为0.1 mol·L-1和0.3 mol·L-1的AlCl3、NH4Cl的混合溶液中加入0.1 mol·L-1的NaOH溶液,发生的反应依次是Al3++3OH-===Al(OH)3↓、OH-+NH
参加反应,再加1.5 L H2SO4时,Al(OH)3全部溶解,A正确;B项,向1 L浓度分别为0.1 mol·L-1和0.3 mol·L-1的AlCl3、NH4Cl的混合溶液中加入0.1 mol·L-1的NaOH溶液,发生的反应依次是Al3++3OH-===Al(OH)3↓、OH-+NH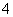 ===NH3·H2O、Al(OH)3+OH-===AlO
===NH3·H2O、Al(OH)3+OH-===AlO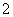 +2H2O,所以沉淀Al3+和溶解Al(OH)3所用NaOH的量之比为3∶1,而图像上看到的是1∶1,B错误;C项,向烧碱溶液中滴加明矾溶液,发生的反应依次是Al3++4OH-===AlO
+2H2O,所以沉淀Al3+和溶解Al(OH)3所用NaOH的量之比为3∶1,而图像上看到的是1∶1,B错误;C项,向烧碱溶液中滴加明矾溶液,发生的反应依次是Al3++4OH-===AlO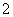 +2H2O、Al3++3AlO
+2H2O、Al3++3AlO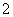 +6H2O===4Al(OH)3↓,C错误;D项,AlCl3溶液中滴加过量氨水,沉淀不会溶解,D错误。
+6H2O===4Al(OH)3↓,C错误;D项,AlCl3溶液中滴加过量氨水,沉淀不会溶解,D错误。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列哪些事实或实验能说明氧化性:Cl2>Br2>I2_____________________________________________________________________
(填序号)。
①氯水分别滴入KBr、NaI溶液中颜色加深,而溴水滴入NaCl溶液中无明显变化,滴入KI淀粉溶液中,溶液变蓝
②H2和Cl2的混合气体光照爆炸,H2和Br2的混合气体加热才能反应,而H2和I2反应更困难
③Fe分别与Cl2、Br2、I2反应生成Fe的化合物的化合价高低
④HCl、HBr、HI的热稳定性越来越差
⑤Cl2、Br2、I2在水中的溶解度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)19世纪末,人们开始揭示原子内部的秘密,最早发现电子的科学家是________。
(2)道尔顿的原子学说曾起了很大的作用。他的学说包含下列三个论点:①原子是不能再分的粒子,②同种元素的原子的各种性质和质量都相同,③原子是微小的实心球体。从现代的观点看,你认为三个论点中不确切的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色溶液中:ClO-、MnO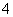 、Al3+、K+
、Al3+、K+
B.1.0 mol·L-1的NaAlO2溶液中:Cl-、HCO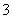 、K+、Ca2+
、K+、Ca2+
C.在强碱性环境中:AlO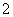 、SiO
、SiO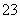 、Na+、K+
、Na+、K+
D.能使甲基橙显红色的溶液中:NH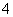 、AlO
、AlO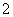 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
铝土矿的主要成分为氧化铝、氧化铁和二氧化硅,工业上经过下列工艺可以冶炼金属铝:
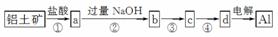
下列说法中错误的是( )
A.①②中除加试剂外,还需要进行过滤操作
B.a、b中铝元素的化合价相同
C.③中需要通入过量的氨气
D.④进行的操作是加热,而且d一定是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2 800 | 2 050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是__________________________;
制铝时,电解Al2O3而不电解AlCl3的原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
金属钠着火,不能用H2O、干冰灭火的原因是_____________________________________,
通常用__________掩埋。
查看答案和解析>>
科目:高中化学 来源: 题型:
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠________g。
(2)钠钾合金可在核反应堆中用作热交换液。5.05 g钠钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
②计算并确定该钠钾合金的化学式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com