
| A、标准状况下NA个SO3的体积为22.4 L |
| B、1mol Fe与足量的HCl反应,转移的电子数为3NA |
| C、2L 1mol/L的 H3PO4溶液中所含的H+数为6NA |
| D、标准状况下22.4L Cl2通入足量的石灰乳制备漂白粉,转移电子数为1 NA |


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
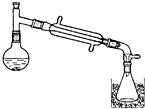 一溴乙烷为无色液体,熔点-119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷
一溴乙烷为无色液体,熔点-119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷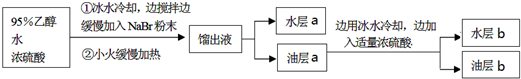
| 实验步骤 | 预期现象和结论 |
| 步骤1:将油层b转移至 | |
| 步骤2:取步骤1的水层少量于试管中,加入稀硫酸酸化,再加入适量新制氯水及少量CCl4,充分振荡,静置. | 溶液分层,下层呈橙红色,证明 |
| 步骤3:将步骤1的油层充分洗涤、干燥后装入蒸馏装置中, | 馏出蒸汽的温度稳定在38℃左右,不再有蒸汽馏出时,将蒸馏烧瓶中残留液体置于冰水浴中冷却,凝结成白色固体,则证明油层b中含有1,2-二溴乙烷. |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO- 4 |
2- 4 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去N2中的少量O2:通过灼热的CuO粉末,收集气体 |
| B、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| C、除去CO2中的少量HCl:通入Na2CO3溶液,收集气体 |
| D、除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,2.24LH2O含有的质子数为NA |
| B、等物质的量的氮气和氧气,都含有2NA个原子 |
| C、常温常压下,1.06gNa2CO3含有的Na+离子数为0.02 NA |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有HCO3-或CO32- |
| B、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| C、欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
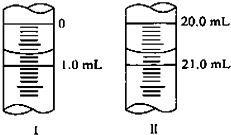
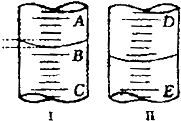 (如图)(1)图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是
(如图)(1)图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com