
【题目】关于热化学方程式:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,下列有关叙述不正确的是( )
A.上述热化学方程式可表示为H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
B.1 mol H2完全燃烧生成液态水时放出285.8 kJ的热
C.2个氢分子完全燃烧生成液态水时放出571.6 kJ的热
D.2 mol H2完全燃烧生成液态水放出571.6 kJ的热
【答案】C
【解析】
燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,氢气的燃烧热为258.8 kJmol-1,据此进行分析。
A.H2(g)+ ![]() O2(g)=H2O(l);△H=-258.8 kJmol-1 ,符合燃烧热概念,故A正确;
O2(g)=H2O(l);△H=-258.8 kJmol-1 ,符合燃烧热概念,故A正确;
B.燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,所以1 mol H2完全燃烧生成液态水时放出285.8 kJ的热量,故B正确;
C.化学计量数表示的是参加反应的物质的物质的量,不是分子数,应该是2mol氢气完全燃烧生成液态水时放出571.6 kJ的热量,故C错误;
D.根据氢气燃烧的热化学方程式可知,2mol H2完全燃烧生成液态水放出571.6 kJ的热量,故D正确;
故选C。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】高铁电池是电动汽车首选的电池之一,该电池的工作原理为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,
3Zn(OH)2+2Fe(OH)3+4KOH,
下列关于该电池放电时的说法中正确的是( )
A.高铁电池产生的电流从负极经外电路到达正极
B.正极反应式为Zn+2OH--2e- =Zn(OH)2
C.负极pH减小,正极pH增大,电解液pH增大
D.每氧化1mol高铁酸钾转移3mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于四种仪器装置的有关用法中不合理的是( )
A.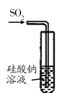 装置:可用来证明硫的非金属性比硅强
装置:可用来证明硫的非金属性比硅强
B.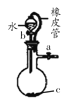 装置:橡皮管的作用是能使水顺利流下
装置:橡皮管的作用是能使水顺利流下
C.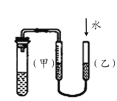 装置:用图示的方法能检查此装置的气密性
装置:用图示的方法能检查此装置的气密性
D. 装置:可在瓶中先装满水,气体由
装置:可在瓶中先装满水,气体由![]() 口入,收集NO气体
口入,收集NO气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,已知:NaClO2饱和溶液在温度低于38℃时析出晶体NaClO2![]() ,温度高于38℃时析出晶体NaClO2,温度高于60℃时NaClO2分解生成NaClO3和
,温度高于38℃时析出晶体NaClO2,温度高于60℃时NaClO2分解生成NaClO3和![]() 。其一种生产工艺如下。
。其一种生产工艺如下。

请回答下列问题:
(1)NaClO2中![]() 的化合价为_____________。
的化合价为_____________。
(2)反应I:
①![]() 做___________(填“氧化剂”或“还原剂”)。
做___________(填“氧化剂”或“还原剂”)。
②将反应I中的化学方程式补充完整:
![]() _____________
_____________
(3)电解II:
①所用食盐水由粗盐水精制而成,精制时,为除去粗盐水中的![]() 和
和![]() ,需要加入的试剂分别为_______、___________。
,需要加入的试剂分别为_______、___________。
②电解过程中被氧化的物质是________。
③可用![]() 溶液吸收电解产生的
溶液吸收电解产生的![]() ,该反应的离子方程式是______________。
,该反应的离子方程式是______________。
(4)操作III:
滤液获利NaClO2的操作步骤:①加热蒸发;②趁热过滤;③洗涤;④干燥,得到成品。趁热过滤应控制的温度范围是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量,某兴趣小组进行下面实验探究,查阅资料知道:
①2NO + Na2O2=2NaNO2
②2NO2+ Na2O2=2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-还原成Mn2+。
Ⅰ.产品制备与检验:用如下装置制备NaNO2:
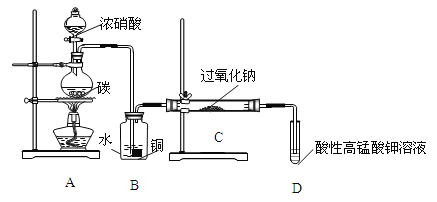
(1)写出装置A烧瓶中发生反应的化学方程式并标出电子转移的方向和数目________。
(2)B装置的作用是______________________________。
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净NaNO2应在B、C装置间增加一个装置,请在框内画出增加的装置图,并标明盛放的试剂________。

(4)试设计实验检验装置C中NaNO2的存在(写出操作、现象和结论)________。
Ⅱ.含量的测定
称取装置C中反应后的固体4.000g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
(5)第一组实验数据出现异常,造成这种异常的原因可能是________(双项选择)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
D.滴定终了俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数____________________。
(结果保留4位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 是一种在药物合成中有重要作用的有机物,下列关于该有机物的说法正确的是
是一种在药物合成中有重要作用的有机物,下列关于该有机物的说法正确的是
A.该有机物在一定条件下能发生酯化反应、还原反应、氧化反应、加成反应、消去反应
B.该有机物中有4种官能团
C.1mol该有机物分别与足量的碳酸氢钠溶液、金属钠反应,产生气体的物质的量不相同
D.该有机物的分子式为C14H16O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员以Zn和尖晶石型锰酸锌( ZnMn2O4)为电极材料,研制出一种水系锌离子电池,该电池的总反应式为xZn+Zn1-xMn2O4![]() ZnMn2O4(0<x<1)。下列说法正确的是( )
ZnMn2O4(0<x<1)。下列说法正确的是( )
A.放电时,Zn2+向负极迁移
B.充、放电过程中,仅锌元素的价态发生变化
C.充电时,阳极的电极反应式为ZnMn2O4 -2xe-=Zn1-XMn2O4+xZn2+
D.若维持电流强度为0.5A,放电10分钟,理论上消耗Zn的质量约为0.20 g (已知F =96500 C/mol)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.1mol/L的NaOH溶液,分别滴定20mL、浓度均为0.1mol/L的两种酸HX、HY。所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是

A.0.1mol/L的一元酸HY在水中有1%发生电离
B.a点的导电能力比b点弱
C.b点溶液中,c(HY)+2c(H+)=c(Y-)+2c(OH-)
D.加NaOH溶液至pH=7时,两种溶液中,(X-)=c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C8H8的两种同分异构体X和Y。Y是一种芳香烃,分子中只有一个环;X俗称立方烷,其核磁共振氢谱显示只有一个吸收峰。下列有关说法错误的是( )
A.X、Y均能燃烧,都有大量浓烟产生
B.X既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,还能发生加聚反应
C.Y属于不饱和烃
D.X的二氯代物有三种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com