
| OH- |

 ,②W为高分子,则W为
,②W为高分子,则W为 ,据此答题.
,据此答题. ,C+E→W的化学方程式为
,C+E→W的化学方程式为 ,
, ;
;  ,C+E→W的化学方程式为
,C+E→W的化学方程式为 ,
, .
.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
A、核素
| ||||
| B、“水玻璃”是硅酸钠的俗称,是一种黏合剂 | ||||
| C、KIO3中碘元素的化合价是+5,碘原子的最外层最多可排7个电子 | ||||
D、I和
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、氢化物的沸点为HnT<HnQ |
| B、L、R的单质与稀盐酸反应的速率为R>L |
| C、M与T形成的化合物具有两性 |
| D、L、Q形成的简单离子的核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
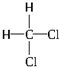 和
和
2 1 |
1 1 |
 和
和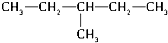
 CH2=CH-CH2CH3 和 CH3-CH=CH-CH3
CH2=CH-CH2CH3 和 CH3-CH=CH-CH3 纤维素与淀粉.
纤维素与淀粉.查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组通过查阅资料得到如下信息,乙醇在加热条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如表所示.
某研究性学习小组通过查阅资料得到如下信息,乙醇在加热条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如表所示.| 溶解性(本身均可做溶剂) | 沸点(℃) | 密度(g/mL) | |
| 乙醇 | 与水混溶,易溶于有机溶剂 | 78.5 | 0.8 |
| 溴乙烷 | 难溶于水,易溶于有机溶剂 | 38.4 | 1.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com