
| A. | 元素C、D、E的最高价氧化物对应水化物的酸性递减 | |
| B. | 元素D、E分别与元素A形成化合物的稳定性:A2D>AE | |
| C. | D、E简单离子的还原性顺序为:D>E | |
| D. | 元素B、D、E的简单离子半径大小为:B>D>E |
分析 五种短周期主族元素A、B、C、D、E的原子序数依次递增,A2属于绿色燃料,则A为H元素;C的氧化物常用于玻璃的生产,则C为Si元素;D元素原子的核电荷数是同主族上一周期元素的2倍,则D为S元素;E的原子序数大于S,则E为Cl元素;B、C为同周期元素,则B位于第三周期,B、D原子最外层电子数之和等于E的最外层电子数,则B最外层电子数=7-6=1,为Na元素,结合对应单质、化合物的性质以及元素周期率解答该题.
解答 解:由以上分析可知A为H、B为Na、C为Si、D为S、E为Cl元素,
A.非金属性Cl>S>Si,元素的非金属性越强,对应的最高价氧化物对应水化物的酸性越强,故A错误;
B.非金属性Cl>S,元素的非金属性越强,对应的氢化物越稳定,故B错误;
C.非金属性Cl>S,元素的非金属性越强,对应的阴离子的还原性越弱,则S、Cl简单离子的还原性顺序为S2->Cl-,故C正确;
D.S2-、Cl-比Na+多一个电子层,Na+半径最小,具有相同核外电子排布的离子,核电荷数越大离子半径越小,应为S2->Cl->Na+,故D错误.
故选C.
点评 本题考查了原子结构与元素周期律的关系,为高频考点,题目难度中等,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,23gNO2和N2O4混合气体中含O原子数为NA | |
| B. | 1mol/L Al2(SO4)3溶液中含SO42-个数为3NA,含Al3+个数小于2NA | |
| C. | 在标准状况下,将22.4L SO3溶于水配成1L溶液,所得溶液中含SO42-个数为NA | |
| D. | 将1moL 氯气通入到足量水中,则N(HClO)+N(Cl-)+N(ClO-)═2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
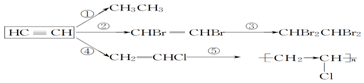
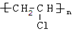 ,加聚反应.
,加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
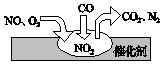 随着我国汽车年销量的大幅增加,空气环境受到了很大的污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
随着我国汽车年销量的大幅增加,空气环境受到了很大的污染.汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )| A. | 反应中NO为氧化剂,N2为氧化产物 | |
| B. | 汽车尾气的主要污染成分包括CO、NO和N2 | |
| C. | NO和O2必须在催化剂表面才能反应 | |
| D. | 催化转化总化学方程式为2NO+O2+4CO=4CO2+N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
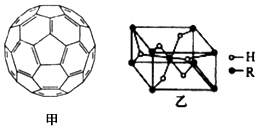
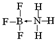 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.00mol NaCl中含有NA个NaCl 分子 | |
| B. | 常温常压下,22.4LCl2与足量镁粉反应,转移的电子数为2NA | |
| C. | 一定条件下,2.3gNa与足量O2完全反应生成3.6g产物时失去的电子数为0.1NA | |
| D. | 28g乙烯和环丙烷(C3H6)组成的混合气体中含有氢原子的个数为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
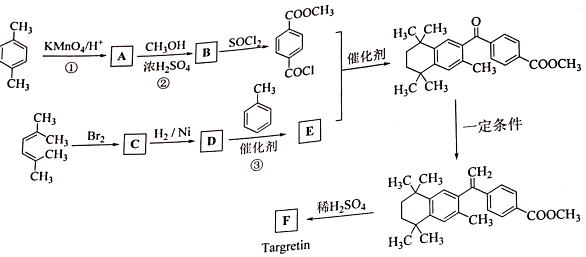
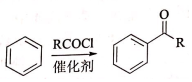 ②
②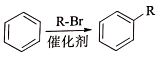
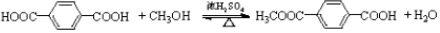 .
.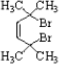 .
.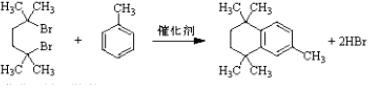 .
. 结构)
结构)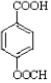 ,
, .
.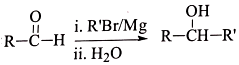 R-CH-R′(R、R′为烃基)
R-CH-R′(R、R′为烃基) ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实 验 Ⅰ | 操作 | 现象 |
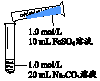 | 1、混合后出现白色絮状沉淀,振荡,部分沉淀呈灰绿色,无气泡产生 2、放置5-8分钟,灰绿色沉淀逐渐增多,最终变成红褐色 |
| 实验Ⅱ | 操作 | 现象 |
 | 1、混合后,试管中出现白色颗粒状浑浊,片刻后有大量气泡产生 2、振荡,粘附在试管内壁的白色颗粒状浑浊变红棕色,且越来越多;20分钟后,白色浑浊明显沉降 |
| 实验Ⅱ | 操作 | 现象 |
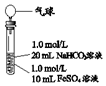 | 1、混合后,试管中出现白色颗粒状浑浊,片刻后有大量气泡产生 2、一段时间后将带有气球(排尽空气)的胶塞塞紧试管,振荡后放置5小时,气球膨胀,试管中沉淀物始终保持白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中的溴(碘化钾溶液) | B. | 汽油中的苯(水) | ||
| C. | 煤焦油中的苯、甲苯、二甲苯(分液) | D. | 甲烷中的乙烯(溴水) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com