
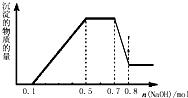
 溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )| A、溶液中一定不含CO32-,可能含有SO42-和NO3- |
| B、在滴加NaOH溶液物质的量为0.5至0.7mol时,发生的离子反应为:Al3++4OH-=AlO2-+2H2O |
| C、溶液中的阳离子只有H+、Mg2+、Al3+ |
| D、n(H+):n(NH4+):n(Mg2+)=2:4:1 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、乙烯与Br2发生加成反应生成CH3CHBr2 |
| B、酸性高锰酸钾溶液可确定苯和乙醇的混合液中混有乙醇 |
| C、葡萄糖、油脂、蛋白质都是可水解的高分子化合物 |
| D、乙烯和苯都是平面结构,因为二者分子中都含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
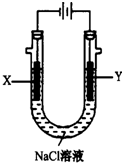 甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、①③ | B、②④ | C、①④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B、常温下浓硫酸与铝不反应,可用铝槽车运输 |
C、二氧化碳的电子式: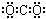 |
| D、Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.8 g D2O含有NA个中子 |
| B、用5 mL 3 mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015 NA |
| C、在Na2O2与CO2的反应中,每转移NA个电子时,消耗22.4 L的CO2 |
| D、25℃时,7 g C2H4和C3H6的混合气体中,含有NA个C-H键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
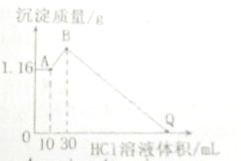 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浑浊液中逐滴加入1mol?L-1HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如下图所示.请回答
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浑浊液中逐滴加入1mol?L-1HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如下图所示.请回答查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-═BaSO4↓ |
| B、双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-═I2+2H2O |
| C、用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com