
| A. | O2-、Cl-、K+ | B. | Cl-、Na+、Al3+ | C. | Na+、Mg2+、F- | D. | O2-、Mg2+、Cl- |
分析 电子层结构完全相同是指电子层数相同,每层上所含电子数相等,结合原子核外电子排布规律进行判断.
解答 解:A.O2-离子含有2个电子层,而Cl-、K+离子都是三个电子层,各层上的电子数分别为2、8、8,电子层结构不完全相同,故A错误;
B.Cl-离子含有三个电子层,各层上的电子数分别为2、8、8,而Na+、Al3+含有2个电子层,电子层结构不完全相同,故B错误;
C.Na+、Mg2+、F-都含有二个电子层,各层上的电子数都分别为2、8,电子层结构完全相同,故C正确;
D.O2-、Mg2+含有二个电子层,Cl-含有三个电子层,电子层结构不完全相同,故D错误;
故选C.
点评 本题考查电子层结构,题目难度不大,明确电子层结构完全相同是指电子层数相同、每层上所含电子数相等是解题的关键,注意掌握核外电子排布规律,试题培养了学生的灵活应用能力.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| B. | 往蔗糖与稀硫酸共热后的溶液中滴加银氨溶液,再水浴加热,能看到银镜生成 | |
| C. | 淀粉和纤维素的分子式均为(C6H10O5)n,二者互为同分异构体 | |
| D. | 向鸡蛋清溶液中加硫酸铵饱和溶液,有沉淀析出,再加水沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 甲中试剂 | 乙中试剂 | 气体成份及实验目的 | 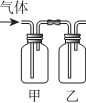 |
| A | NaHSO3溶液 | 硅酸钠溶液 | HCl:证明非金属Cl>S>Si | |
| B | FeI2淀粉溶液 | FeI2、KSCN溶液 | Cl2:验证氧化性Cl2>Fe3+>I2 | |
| C | 溴水 | AgNO3溶液 | 乙烯:验证溴水与乙烯发生的是加成反应 | |
| D | Ba(OH)2溶液 | 品红溶液 | 验证混合气体中含有SO2和CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
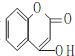 )的路线如下图所示:
)的路线如下图所示: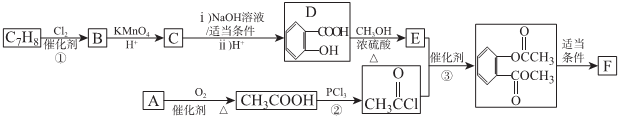
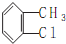 .
.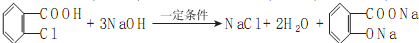 .
.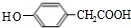 .
.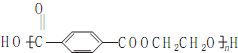 ),参照A→乙酸的表示方法,写出相应的合成路线图
),参照A→乙酸的表示方法,写出相应的合成路线图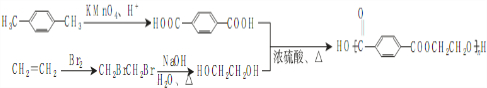 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(甲)>v(乙)>v(丙) | B. | v(乙)>v(丙)>v(甲) | C. | v(丙)>v(乙)>v(甲) | D. | v(乙)>v(甲)>v(丙) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
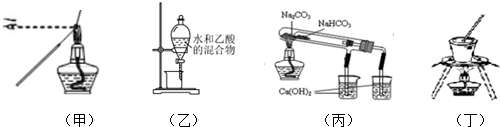
| A. | 甲图装置:用蘸有待测液的铁丝,检验K+ | |
| B. | 乙图装置:分离水和乙酸 | |
| C. | 丙图装置:验证NaHCO3和Na2CO3的热稳定性 | |
| D. | 丁图装置:从食盐水中提取食盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
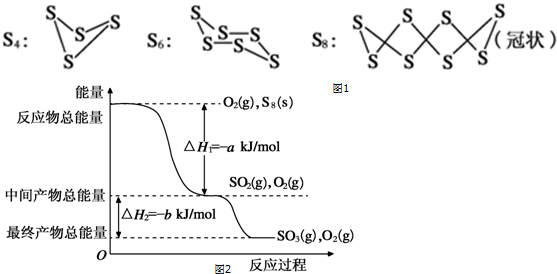
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳和环氧丙烷在催化作用下可生成一种可降解的高聚物,可减少二氧化碳对环境的影响 | |
| B. | 化石燃料的燃烧和含硫金属矿石的冶炼等都是造成SO2污染的重要原因 | |
| C. | 氟氯烃的大量使用会破坏臭氧层,火箭、导弹将大量废气排放到高空,也会加速臭氧分解 | |
| D. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com