
在①MgO、CuO、CaO、SO2;②C、Fe、S、P;③ZnCl2、BaCO3、HNO3、NaNO3三组物质中,每组各有一种物质在分类上与组内其他物质不同,这三种物质分别是( )
A.CuO、Fe、ZnCl2 B. SO2 、Fe、HNO3 C. CaO、C、BaCO3 D. SO2 、S、NaNO3
科目:高中化学 来源: 题型:
在一定条件下,下列粒子的还原性顺序:Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是 ( )
A.2Fe3++SO2+2H2O===2Fe2++SO42-+4H+
B.2Br-+4H++SO42-===SO2+Br2+2H2O
C.2Fe2++Cl2===2Fe3+2Cl-
D.I2+SO2+2H2O===4H++SO42-+2I-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质或应用的说法不正确的是
A.水玻璃可用于生产黏合剂和防火剂
B.小苏打用于治疗胃溃疡病人的胃酸过多症
C.盐析可提纯蛋白质并保持其生理活性
D.FeCl3 溶液能与Cu 反应,可用于蚀刻印刷电路
查看答案和解析>>
科目:高中化学 来源: 题型:
进行化学实验必须注意安全,下列说法不正确的是( )
A.不慎将酸溅到眼中,应立即用大量水冲洗,边洗边眨眼睛
B.不慎将浓碱溶液沾到皮肤上,应立即用大量的水冲洗
C.加热试管或烧杯时,应首先擦干外壁上的水
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
A.1 mol NH3所含有的原子数为NA
B.常温常压下,22.4L氧气所含的原子数为2NA
C.常温常压下,48gO2和O3的混和物中所含氧原子数为3NA
D.1 L 0.1 mol/LNaCl溶液中所含的Na+为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
有28gCuO和MgO固体混合物与200ml硫酸恰好完全反应,将反应后的溶液小心蒸干,得到固体68g。则原硫酸溶液的物质的量浓度和原固体混合物中氧元素的质量分数分别是( )
A.2.5mol•L-1 28.57% B. 2.2mol•L-1 23.07%
C. 1.5mol•L-1 24.55% D.2.5mol•L-1 18.37%
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.滴入酚酞呈无色的溶液中:K+、Al3+、Cl-、CO32-
B.澄清的溶液中:Na+、K+、MnO4—、AlO2—
C. =10-13 mol·L-1的溶液:Na+、[Ag(NH3)2]+、OH-、NO3-
=10-13 mol·L-1的溶液:Na+、[Ag(NH3)2]+、OH-、NO3-
D.c(I-)=0.1 mol·L-1的溶液中:Na+、H+、ClO-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
镁是海水中含量较多的金属,镁合金及其镁的化合物用途非常广泛。
(1)Mg2Ni是一种储氢合金,已知:
Mg(s) + H2(g) = MgH2(s) △H1=-74.5kJ·mol-1
Mg2Ni(s) + 2H2(g) = Mg2NiH4(s) △H2=-64.4kJ·mol-1
Mg2Ni(s)+2MgH2(s) = 2Mg(s)+Mg2NiH4(s) 的△H3= ▲ 。
(2)一种用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁工艺的关键流程如下:

①为探究MgCl2•6H2O“一段脱水”的合理温度范围,某科研小组将MgCl2•6H2O在不同温度下分解,测得残留固体物质的X-射线衍射谱图如下图所示(X-射线衍射可用于判断某晶态物质是否存在)。
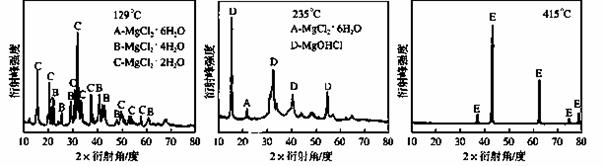
测得E中Mg元素质量分数为60.0%,则E的化学式为 ▲ 。
“一段脱水”的目的是制备MgCl2·2H2O,温度不高于180 ℃的原因是 ▲ 。
 ②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率。生成MgO的化学方程式为 ▲ 。
②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率。生成MgO的化学方程式为 ▲ 。
③该工艺中,可以循环使用的物质有 ▲ 。
(3)储氢材料Mg(AlH4)2在110-200°C的反应为:
Mg(AlH4)2=MgH2 +2A1+3H2↑
每生成27gAl转移电子的物质的量为 ▲ 。
(4)“镁-次氯酸盐”燃料电池的装置如右图所示,该电池的正极反应式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:
3A(g)+B(g) 2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
(1)用C表示10s内正反应的平均反应速率为: ;
(2)反应前A的物质的量浓度是: ;
(3)10s末,生成物D的浓度为 ;
(4)平衡后,若改变下列条件,生成D的速率如何变化(用“增大”、“减小”或 “不变”填空)。
| 编号 | 改变的条件 | 生成D的速率 |
| ① | 降低温度 | |
| ② | 增大A的浓度 | |
| ③ | 使用催化剂 | |
| ④ | 增大压强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com