
反应4NH3(g)+5O2(g)4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均反应速率v(X)(反应物的消耗速率或产物的生成速率)可表示为( )
A.v(O2)=0.001 mol·L-1·s-1
B.v(NH3)=0.01 mol·L-1·s-1
C.v(NO)=0.001 mol·L-1·s-1
D.v(H2O)=0.045 mol·L-1·s-1
科目:高中化学 来源: 题型:
25 ℃时,PbCl2固体在不同浓度盐酸中的溶解度曲线如图。在制备PbCl2的实验中,洗涤PbCl2固体最好选用( )
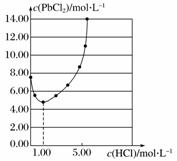
A.蒸馏水
B.1.00 mol·L-1盐酸
C.5.00 mol·L-1盐酸
D.10.00 mol·L-1盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气,某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气。供选用的实验试剂及装置如下图所示(部分导管、蒸馏水略)。
a.Na2O2 b.浓盐酸 c.碱石灰 d.NaOH溶液 e.淀粉KI溶液 f.CaCO3 g.石蕊溶液 h.饱和NaCl溶液
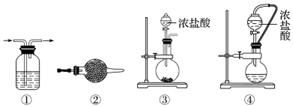
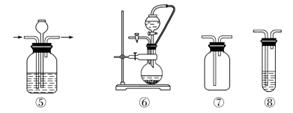
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式:__________________________
________________________________________________________________________
________________________________________________________________________。
(2)下表中的装置组合最合理的是__________(填字母,需考虑实验结束撤除装置时残留有害气体的处理)。
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/g | ① |
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为________________________________________________________________________。
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①________________________________________________________________________;
②________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知分解1 mol H2O2放出热量98 kJ,在含少量I-的溶液中,H2O2分解的机理为
H2O2+I-—→H2O+IO- 慢
H2O2+IO-—→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
A.反应速率与I-浓度有关
B.IO-也是该反应的催化剂
C.反应活化能等于98 kJ·mol-1
D.v(H2O2)=v(H2O)=v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
催化反硝化法可用于治理水中硝酸盐的污染,H2能将NO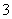 还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12,上述反应的离子方程式为________________________________________________________________________
还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12,上述反应的离子方程式为________________________________________________________________________
________________________________________________________________________,
其平均反应速率v(NO )为________ mol·L-1·min-1。
)为________ mol·L-1·min-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
在298 K时,实验测得溶液中的反应:H2O2+2HI===2H2O+I2在不同浓度时的化学反应速率如表所示,由此可推知第5组实验中c(HI)、c(H2O2)不可能为( )
| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 |
| c(HI)/mol·L-1 | 0.100 | 0.200 | 0.150 | 0.100 | ? | 0.500 |
| c(H2O2)/mol·L-1 | 0.100 | 0.100 | 0.150 | 0.200 | ? | 0.400 |
| v/mol·L-1·s-1 | 0.007 60 | 0.015 2 | 0.017 1 | 0.015 2 | 0.022 8 | 0.152 |
A.0.150 mol·L-1、0.200 mol·L-1
B.0.300 mol·L-1、0.100 mol·L-1
C.0.200 mol·L-1、0.200 mol·L-1
D.0.100 mol·L-1、0.300 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是________________(用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是______________。
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是________________。
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是__________。
(5)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为____________,反应所需时间的长短关系是__________。
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是________________________________________________________________________。
(7)将c(H+)相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L HCl溶液和20.00 mL 0.1000 mol/L CH3COOH溶液,得到2条滴定曲线,如下图所示:
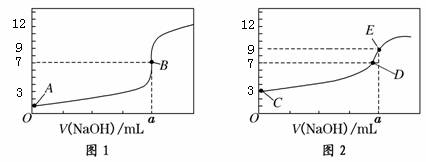
以下说法正确的是( )
A.图1是滴定CH3COOH 溶液的曲线
B.图2若用甲基橙作指示剂达到滴定终点时,则溶液由黄色变为红色
C.点D所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.如果C、E两点对应的pH分别为3、9,则水电离的氢离子浓度之比为1∶100
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com