
 如图是初中化学中常见物质间的转化关系.其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体;乙和丁为黑色固体.
如图是初中化学中常见物质间的转化关系.其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体;乙和丁为黑色固体.分析 (1)甲、乙、丙均为非金属单质;A、B、E和丁均为化合物,乙和丁为黑色固体,B和E为能产生温室效应的气体,根据转化关系,丙与E反应生成B和A,则B为二氧化碳,E为甲烷,所以A为水,丙为氧气,甲乙为非金属单质,反应后能生成水,则甲为氢气,丁是黑色固体,与甲生成水,与乙生成二氧化碳,则丁为氧化铜,乙为碳,将推导出的各物质代入图中验证即可;
(2)根据(1)中的推导及转化关系等,继续推断得出的丙和E的结果,书写化学方程式.
解答 解:(1)甲、乙、丙均为非金属单质;A、B、E和丁均为化合物,乙和丁为黑色固体,B和E为能产生温室效应的气体,根据转化关系,丙与E反应生成B和A,则B为二氧化碳,E为甲烷,所以A为水,丙为氧气,甲乙为非金属单质,反应后能生成水,则甲为氢气,丁是黑色固体,与甲生成水,与乙生成二氧化碳,则丁为氧化铜,乙为碳,综合以上分析,甲为氢气H2、乙为C,
故答案为:H2;C;
(2)根据(1)的推到可知丙是氧气,E为甲烷,反应的化学方程式为CH4+2O2 $\stackrel{点燃}{→}$CO2+2H2O,
故答案为:CH4+2O2 $\stackrel{点燃}{→}$CO2+2H2O.
点评 在解此类题时,主要是找出题中的突破点,而本题的突破点就是B和E为能产生温室效应的气体及乙和丁为黑色固体,题目难度中等.


科目:高中化学 来源: 题型:多选题
| A. | $\frac{12a}{b}$ | B. | $\frac{12b}{a}$ | C. | NA•a | D. | 12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
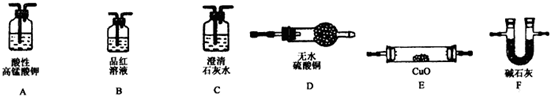
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液分层,上层无色,下层紫红色 | B. | 溶液不分层 | ||
| C. | 溶液分层,上层紫红色,下层无色 | D. | 溶液分层,上层黄色,下层紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9:8 | B. | 11:12 | C. | 12:11 | D. | 3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图I中,甲、乙的平衡常数分别为K1、K2,则K1=K2 | |
| B. | 图Ⅱ中,平衡状态甲与乙相比,平衡状态甲的反应物转化率低 | |
| C. | 图Ⅱ中,t时间是增大了压强 | |
| D. | 图Ⅲ是反应分别在甲、乙条件下达到平衡,说明甲温度高于乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LNO与CO2的混合气体中含有O原子数为3NA | |
| B. | 0.1mol NH3溶于足量水中(不考虑氨气挥发),溶液中N原子的数目为0.1NA | |
| C. | 0.1molN2与足量的H2反应,转移的电子数是0.6NA | |
| D. | 58.5 g的NaCl固体中含有NA个氯化钠分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若起始加入2molN2和6molH2发生反应,则平衡时N2和H2的转化率相同 | |
| B. | 该反应采用高温条件,有利于提高NH3的产率,从而提高生产效率 | |
| C. | 若起始加入2molN2和6molH2发生反应,平衡时测得反应共放热46kJ,则N2的平衡转化率为50% | |
| D. | 若平衡时保持其它条件不变,压缩容器体积,则平衡正向移动,N2的浓度减小,NH3的浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40gNaOH溶于1L水所得的溶液 | |
| B. | 将22.4LHCl溶于水配成1L溶液 | |
| C. | 1L含2mol K+的K2SO4溶液 | |
| D. | 将0.5mol•L-1的NaNO3溶液100mL加热蒸发掉50g水后的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com