
| A、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA |
| B、在标准状况下,22.4L水的质量约为18g |
| C、22g二氧化碳与标准状况下11.2LHCl含有相同的分子数 |
| D、22.4L氮气含氮分子数为NA |


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
| A、冶炼金属铝通常用电解氯化铝的方法 |
| B、要使海水淡化通常有蒸馏法和离子交换法 |
| C、用H2作为燃料的优点之一是燃烧后的产物不污染环境 |
| D、煤的干馏属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol二氧化硅晶体中含有4NA个硅氧键 |
| B、100mL 18.4mo1?L-1硫酸与足量Cu反应,生成SO2的分子数为0.92NA |
| C、0.1L 3mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
| D、将0.l mol FeC13滴入沸水中可制得0.1NA Fe(OH)3胶粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
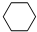 (g)
(g)| FeSO4/Al2O3 |
| 高温 |
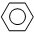 (g)+3H2(g)
(g)+3H2(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由上述反应可知,受热时C4H10比C4H6更难分解 |
| B、1,3-丁二烯比2-丁炔稳定 |
| C、1,3-丁二烯转化为2-丁炔要吸收热量 |
| D、1mol 1,3-丁二烯气体比1mol 2-丁炔气体储存的能量低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | NO3- | SO42- | H+ | M |
| 浓度/mol?L-1 | 2 | 1 | 2 | 1 |
| A、Cl- |
| B、Ba2+ |
| C、NO3- |
| D、Mg2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com