
【题目】党的十九大强调树立“社会主义生态文明观”。下列做法不应该提倡的是( )
A.研发可降解高分子材料,缓解白色污染问题
B.扩大铅蓄电池、含汞干电池的生产,满足消费需求
C.采用碳捕集和封存技术,逐步实现二氧化碳零排放
D.大力发展太阳能、风能等清洁能源,减少对化石燃料的依赖
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关Na2CO3和NaHCO3性质的说法中,正确的是( )
A. 热稳定性:Na2CO3<NaHCO3
B. Na2CO3和NaHCO3均可与澄清石灰水反应
C. 相同温度下,在水中Na2CO3的溶解度小于NaHCO3
D. 106 g Na2CO3和84 g NaHCO3分别与过量盐酸反应,放出CO2的质量:Na2CO3>NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如下图所示(气体体积数据已换算成标准状况下的体积)。关于该固体混合物,下列说法正确的是( )

A. 一定含有MgCl2和FeCl2
B. 一定不含FeCl2,可能含有MgCl2和AlCl3
C. 一定含有Al,其质量为4.5 g
D. 一定含有(NH4)2SO4和MgCl2,且物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是________,D是________,G是________,H是________(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:_____________________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为__________________________。
(3)A中元素的原子结构示意图为________________。
(4)上述反应中属于氧化还原反应的是_________(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中Y形管是一种特殊的仪器,通常与其他仪器组合可以进行某些实验探究。利用下图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。回答下列问题:

(1)广口瓶中间那根玻璃管的作用是:__________________________________________。
(2)实验前需要将BaCl2溶液煮沸,其目的是:_________________________________。
(3)甲中发生反应的化学方程式为:____________________________________________。
(4)乙中分别加入一种常用氧化物和一种无色液体,常温下将两者混合可产生一种碱性气体。该反应的化学方程式为:____________________________________________。
(5)实验时,先使甲中产生的足量气体通入BaCl2溶液中,始终无沉淀生成。由此得出的结论是_______。
(6)向上述⑸实验所得溶液中通入乙产生的气体,产生白色沉淀,请写出发生反应的离子方程式:_____。
(7) 请指出该实验的一个不足之处:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对沉淀溶解平衡的描述正确的是( )
A.电解质的溶解开始后,只有电解质的溶解过程,没有电解质的析出过程
B.沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等
C.沉淀溶解达到平衡时,溶液中溶质的各离子浓度相等,且保持不变
D.沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列微粒的电子式:NaOH__________;CS2_________;Na2S_________NH3__________;NH4H________;
(2)用电子式表示下列物质的形成过程MgCl2______________________
(3)现有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl①只由离子键构成的物质是________________。
②只由极性键构成的物质是_______________。
③由极性键和非极性键构成的物质是________________。
④由离子键和极性键构成的物质是________________。
⑤由离子键和非极性键构成的物质是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期。下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物。下列分析正确的是
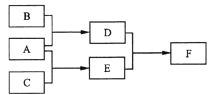
A. Y的氢化物在常温下是液体
B. 与Y同周期氢化物中D最稳定
C. Z的含氧酸均为强酸
D. F含离子键和共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)根据计算用托盘天平需称取氯化钠_________ g;
(2)配制溶液时,除需要烧杯、玻璃棒外,还必须用到的玻璃仪器有 ;
(3)配制溶液有下列几步操作:a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.将溶液移至容量瓶,g.定容.正确的操作顺序是 ;
(4)下列操作结果使溶液物质的量浓度偏低的是___ ______ ;
A.没有将洗涤液转入容量瓶中 |
B.加水定容时,水的量超过了刻度线 |
C.定容时,俯视容量瓶的刻度线 |
D.容量瓶洗涤后,未经干燥处理 |
(5)取出该NaCl溶液10mL加水稀释到200mL,稀释后溶液中NaCl的物质的量浓度是_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com