
| A. | 在强碱溶液中:Na+、K+、CO32-、NO3- | |
| B. | 在pOH=2的溶液中:NH4+、Na+、SO42-、AlO2- | |
| C. | 在pH=1的溶液中:K+、Ag+、Mg2+、Fe2+ | |
| D. | 水电离出来的c(H+)=1×10-13 mol•L-1的溶液:K+、HCO3-、Br-、Ba2+ |
分析 A.强碱性溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
B.该溶液中存在大量氢氧根离子,铵根离子与氢氧根离子、偏铝酸根离子反应;
C.pH=1的溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应;
D.水电离出来的c(H+)=1×10-13 mol•L-1的溶液中存在大量氢离子或氢氧根离子,碳酸氢根离子与氢离子、氢氧根离子反应.
解答 解:A.在强碱溶液中存在大量氢氧根离子,Na+、K+、CO32-、NO3-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故A正确;
B.在pOH=2的溶液呈碱性,溶液中存在大量氢氧根离子,NH4+与OH-、AlO2-发生反应,在溶液中不能大量共存,故B错误;
C.pH=1的溶液中存在大量氢离子,K+、Ag+、Mg2+、Fe2+之间不反应,都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.水电离出来的c(H+)=1×10-13 mol•L-1的溶液呈酸性或碱性,HCO3-与氢离子和氢氧根离子反应,在溶液中不能大量共存,故D错误;
故选AC.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:实验题

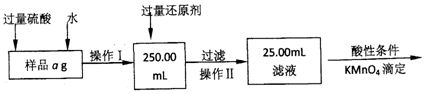
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
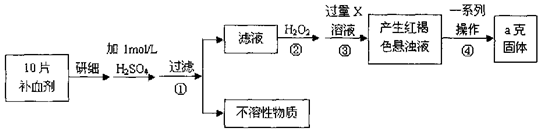
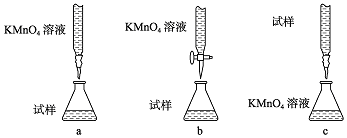
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x=0.6a 2Fe2++Cl2=2Fe3++2Cl- | |
| B. | x=a 2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| C. | x=0.4a 2Br-+Cl2=Br2+2Cl- | |
| D. | x=2a 2Fe2++6Br-+4Cl2=3Br2+2Fe3++8Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Cl>Na>O>N | B. | 碱性:NaOH<Mg(OH)2<Al(OH)3 | ||
| C. | 熔点:CBr4>CCl4>CF4 | D. | 热稳定性:HF>HCl>H2S>H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 900℃时,该反应的平衡常数K<1 | |
| B. | 850℃时,若x=5,则起始时反应向逆反应方向进行 | |
| C. | 850℃时,若要使上述反应开始时向正反应方向进行,则x应满足0≤x<3 | |
| D. | 850℃时,已知x>3,则随着x的增大,H2的转化率一定始终增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 3O2(g)=2O3(g)△H=+242.4kJ•mol-1 | |
| B. | 氧气比臭氧稳定,大气中臭氧层易被破坏 | |
| C. | 断裂l mol O2(g)中的共价键吸收的能量比形成1 molCO2(g)中的共价键放出的能量少 | |
| D. | 相同物质的量的氧气比臭氧所含的能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 用图中的简易装置可以进行气体的发生和收集.
用图中的简易装置可以进行气体的发生和收集.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com