
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有___________________________。
(2)硫酸铜溶液可以加快氢气生成速率的原因是______________________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有______(答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=__________________,V6=__________,V9=________;
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色;
③该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:________________________________________________________________________
________________________________________________________________________。
答案 (1)CuSO4+Zn===ZnSO4+Cu,Zn+H2SO4===ZnSO4+H2↑ (2)CuSO4与Zn反应产生的Cu与Zn可形成CuZn原电池,加快了氢气产生的速率
(3)Ag2SO4 (4)升高反应温度、适当增大硫酸的浓度、增加锌的比表面积等(答两种即可) (5)①30 10 17.5 ②灰黑 暗红 ③当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积而使反应速率下降
解析 (1)在稀硫酸中加入硫酸铜后发生了两个反应:CuSO4+Zn===ZnSO4+Cu、Zn+H2SO4===ZnSO4+H2↑。(2)由于Zn与反应生成的Cu及硫酸铜溶液组成了CuZn原电池,大大加快了生成氢气的反应速率。(3)只要是比锌的金属性弱的金属都可以与锌组成原电池,都可以加快生成氢气的反应速率,故在所给的物质中只有Ag2SO4符合题意。(4)要加快生成氢气的反应速率,还可以采取如下措施:升高温度、适当增大硫酸的浓度、增加锌粒的比表面积等。(5)因为要研究硫酸铜的量对反应速率的影响,故应保持硫酸的浓度在各组实验中相同,则硫酸溶液的体积均取 30 mL,根据F中增加的水与硫酸铜溶液的体积之和为20 mL,可以求得V6=10 mL,V7=20 mL,V8=19.5 mL,V9=17.5 mL,V10=15 mL。当溶液中没有铜析出时,故显示的是锌的颜色:灰黑色,E中析出较多的铜,则显示了铜晶体的颜色:暗红色。由于析出的铜的量较多,会覆盖在锌的表面,使得锌与稀硫酸接触面积大大减小,故反应速率反而减慢。


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则下列叙述中正确的是( )
A.原子序数:D>C>B>A
B.原子半径:B>A>C>D
C.离子半径:C3->D->A2+>B+
D.氧化性:A2+>B+,还原性:C3-<D-
查看答案和解析>>
科目:高中化学 来源: 题型:
油脂皂化后,要使肥皂和甘油从混合物里充分分离,可采用①分液 ②蒸馏 ③过滤 ④盐析 ⑤渗析中的_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有两种戊碳糖,其结构简式分别为HOCH2CHOHCHOHCHOHCHO和
HOCH2CHOHCHOHCH2CHO,它们能发生的化学反应是 ( )
①与氢气在催化剂作用下发生加成反应 ②与氯化铁溶液发生显色反应 ③与新制氢氧化铜在加热条件下发生氧化反应 ④与碳酸氢钠溶液反应产生气泡 ⑤与钠反应 ⑥在浓硫酸、加热条件下发生消去反应
A.①②④⑤ B.②④⑤⑥
C.②④ D.①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中需要22.4 L(标准状况)SO2气体。化学小组同学依据化学方程式Zn+2H2SO4(浓)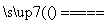 ZnSO4+SO2↑+2H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
ZnSO4+SO2↑+2H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
(1)化学小组所制得的气体中混有的主要杂质气体可能是______(填分子式)。产生这种结果的主要原因是________(用化学方程式和必要的文字加以说明)。
(2)为证实相关分析,化学小组的同学设计了实验,组装了如下装置,对所制取的气体进行探究。
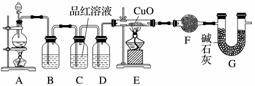
①装置B中加入的试剂为________,作用是________。
②装置D加入的试剂为________________,装置F加入的试剂为________________。
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有某杂质气体的实验现象是________。
④U形管G的作用为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化。
(1)该同学最初的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅰ | 先向2 mL 0.1 mol·L-1 FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | |
| Ⅱ | 先向2 mL 0.1 mol·L-1 FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol·L-1 KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加KI溶液后,血红色无明显变化 |
①实验Ⅰ的现象为________________________________________________________________________。
②FeCl2溶液与新制氯水反应的离子方程式为________________________________________________________________________
________________________________________________________________________。
(2)该同学分析了导致实验Ⅱ现象的可能原因,并对实验方案进行了改进。改进后的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅲ | 向2 mL 0.1 mol·L-1 KI溶液中滴加1 mL | |
| 0.1 mol·L-1 FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
根据实验Ⅲ,该同学认为Fe3+有可能与I-发生氧化还原反应,请结合实验现象用简明的文字说明他得出上述结论的理由:________________________________________________________________________。
(3)该同学认为需要进一步设计实验,证明根据实验Ⅲ中现象得出的结论。请补全下表中的实验方案:
| 编号 | 操作 | 预期现象及结论 |
| Ⅳ | 向2 mL 0.1 mol·L-1 KI溶液中滴加1 mL0.1 mol·L-1 FeCl3溶液,__________ |
(4)上述实验结果表明,Fe3+有可能与I-发生氧化还原反应。进一步查阅资料知,参加反应的Fe3+与I-的物质的量相同。该同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变血红的原因,认为Fe3+与I-反应的离子方程式应写为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知正己烷的球棍模型为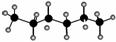 。某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是 ( )。
。某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是 ( )。
A.a分子中可能有三个甲基
B.a的分子式为C6H10
C.a的一氯代物可能有三种
D.在光照条件下,a能与溴的四氯化碳溶液发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”。
(1)离子晶体除含离子键外,一定不含其他化学键(×)
(2)离子晶体中一定含有金属阳离子(×)
(3)离子晶体的熔点一定低于原子晶体(×)
(4)含有阳离子的晶体一定是离子晶体(×)
(5)离子晶体中一定不含分子(×)
(6)金属与非金属形成的化合物一定都是离子化合物(×)
(7)具有金属光泽且能导电的单质一定是金属(×)
(8)金属晶体的熔点差别很大,有的很高(如钨),有的很低(如汞)(√)
查看答案和解析>>
科目:高中化学 来源: 题型:
在等温等容条件下,可逆反应:2A(g)+B(g)3C(g)+D(s)起始物质的量如下表所示:
| 序号 | A | B | C | D |
| ① | 2 mol | 1 mol | 0 | 0 |
| ② | 4 mol | 2 mol | 0 | 0 |
| ③ | 1 mol | 0.5 mol | 1.5 mol | 0.5 mol |
| ④ | 0 | 1 mol | 3 mol | 1 mol |
| ⑤ | 0 | 0 | 3 mol | 1 mol |
上述反应达到平衡时,互为等效平衡的是哪几组?达到平衡后,哪些量相同?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com