
��1����ʱ��Һ����������ǵ�һ�ɷ֣�������____________������Ƕ��ֳɷ֣�������____________��
��2�����������õ���Һ�У���λ����μ����� 1 mol��L-1,�������壨�������ܽ���ˮ������������ӵ�����������ϵ����ͼ��ʾ��
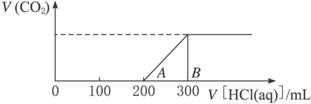
�ټ���200 mL ����֮ǰ�������������д��A��֮ǰ������Ӧ�����ӷ���ʽ___________________________________��
��������Ķ�����̼�ڱ�״���µ�������١�
����B��ʱ����Ӧ������Һ�����ʵ����ʵ���Ũ���Ƕ��١�����Һ����ı仯���Բ��ƣ���
��1��Na2CO3��NaHCO3 NaHCO3,NaOH-Na2CO3,NaHCO3-Na2CO3
(2)��OH-+H+====H2O, ![]() +H+====
+H+====![]()
��2 240 mL ��0.75 mol��L-1
������(1)���������������̼��Ӧ���������У�CO2+2NaOH====Na2CO3+H2O; CO2+NaOH====NaHCO3��̼���ƺ�̼������ˮ��Һ���ʼ��ԣ�����������̼�����Ʋ����档
��2����̼���������H+�ķ�Ӧ�Ƿֲ����еģ���������̼��������ӣ�����̼�������������ķ�Ӧ���ɶ�����̼����ͼ�������֪����̼������������ᷴӦ���ɶ�����̼�����õ�����Ϊ100 mL��˵����Һ��̼���������Ϊ0.1 mol����ԭ��Һ��̼�������Ϊ0.1 mol���������ᷴӦ����̼�����������������100 mL����ͼ������ʾ�����ɶ�����̼֮ǰ����������200 mL���ʷ�Ӧ�����Һ�г�̼��������������ơ�
��![]()
![]() HCl
HCl![]() CO2
CO2
0.1 L��1 mol��L-1 2.24 L
�۷�Ӧ����Һ�е�����ֻ���Ȼ��ƣ�������ԭ���غ����ԭ���غ�ɵã�
NaOH![]() NaCl
NaCl![]() HCl
HCl
0.3 mol 0.3 L��1 mol��L-1
c(NaCl)=0.3 mol/(0.1 L+0.3 L)=0.75 mol��L-1��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ũ�����������������̹�����ȡ���� | B����״���£���1 g��ƬͶ��20 mL 18.4 mol/L�������� | C����100 mL 3 mol/L�������м���5.6 g�� | D�����¡���ѹ���д��������£���1 mol������4 mol�����ϳɰ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����ʱ��Һ����������ǵ�һ�ɷ֣�������________________������Ƕ��ֳɷ֣�������_______________��
��2��������������Һ�У���λ����μ�1 mol��L -1�����ᣬ�������壨�������ܽ���ˮ������������ӵ�����������ϵ����ͼ��ʾ��
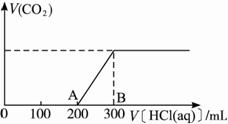
�ټ�������200 mL֮ǰ�������������д��OA�η�����Ӧ�����ӷ���ʽ__________________��
�ڲ�����CO2�ڱ�״���µ����Ϊ_____________mL��
��B��ʱ����Ӧ������Һ�����ʵ����ʵ���Ũ���� ______________mol��L -1(��Һ����ı仯���Բ���)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ2010-2011ѧ�������ѧ�����п��ԣ����ۣ���ѧ���� ���ͣ�ѡ����
�ڸ��������£����мӵ�������ڻ�ѧ��Ӧ���ܱ���ȫ���ĵ��� �� ��
|
A����100 mL 3 moI��L��1���������5.6g�� |
|
B����״���£���1g��ƬͶ��20 mL 18.4mol��L��1�������� |
|
C����50mL 8 mol��L��1Ũ������10g���⻯�̹�����ȡ���� |
|
D����5��l07Pa��500�������ý���������£��������������ϳɰ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�����ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ѡ����
�ڸ��������£����мӵ�������ڻ�ѧ��Ӧ����ȫ���ĵ���
A����50 mL 12 mol/L���Ȼ���ˮ��Һ�������������̹�����ȡ����
B����100 mL 3 mol/L���������5.6 g��
C����״���£���1 g��ƬͶ��20 mL 18.4 mol/L��������
D����5��107Pa��500�������ý���������£�1 mol������3 mol������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�츣��ʡ��һ��ѧ����ĩ������ѧ�Ծ� ���ͣ�ѡ����
�ڸ��������£����л��������ڻ�ѧ��Ӧ���ܱ���ȫ���ĵ���
A����30 ml 12mol/LŨ������8.7g �������̹�����ȡ����
B������£���2.7g ��ƬͶ�뵽20 ml 18 mol/L��Ũ������
C����100 ml 3 mol/L ���������5.6g ��
D����Ba(OH)2��NaOH��0.1mol�Ļ����Һ��ͨ���״����2.8L CO2 ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com