
| A. | 1:3 | B. | 5:1 | C. | 1:1 | D. | 1:2 |
分析 发生的反应有:2Na+2H2O=2NaOH+H2↑、2Na2O2+2H2O=4NaOH+O2↑、2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;根据n=$\frac{V}{{V}_{m}}$分别计算出2.24L、1.12L气体的物质的量,然后得出参加反应的氢气和氧气气体的物质的量,再通过讨论判断氢气和氧气的物质的量,最后根据反应方程式计算出钠、过氧化钠的物质的量及物质的量之比.
解答 解:标准状况下2.24L气体的物质的量为:$\frac{2.24L}{22.4L/mol}$=0.1mol,说明钠、过氧化钠与水反应生成的氢气和氧气的总物质的量为0.1mol,
气体体积减少的1.12L的物质的量为:$\frac{1.12L}{22.4L/mol}$=0.05mol,
则反应后剩余气体的物质的量为:0.1mol-0.05mol=0.05mol,可能为氧气或氢气,
当剩余的0.05mol为氧气时,根据反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O可知,混合气体中含有氢气的物质的量为:0.05mol×$\frac{2}{3}$=$\frac{1}{30}$mol,氧气的体积为:0.1mol-$\frac{1}{30}$mol=$\frac{1}{15}$mol,
根据方程式2Na+2H2O=2NaOH+H2↑、2Na2O2+2H2O=4NaOH+O2↑可知,钠的物质的量为n(Na)=2n(H2)=$\frac{1}{30}$mol×2=$\frac{1}{15}$mol,过氧化钠的物质的量为:n(Na2O2)=2n(O2)=$\frac{2}{15}$mol,原混合物中钠与过氧化钠的物质的量之比为:$\frac{1}{15}$mol:$\frac{2}{15}$mol=1:2,故D正确;
当剩余的0.05mol为氢气时,根据反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O可知,原混合气体中含有氧气的体积为:0.05mol×$\frac{1}{3}$=$\frac{1}{60}$mol,氢气的体积为:0.1mol-$\frac{1}{60}$mol=$\frac{1}{12}$mol,
根据方程式2Na+2H2O=2NaOH+H2↑、2Na2O2+2H2O=4NaOH+O2↑可知,钠的物质的量为n(Na)=2n(H2)=$\frac{1}{12}$mol×2=$\frac{1}{6}$mol,过氧化钠的物质的量为:n(Na2O2)=2n(O2)=$\frac{1}{60}$mol×2=$\frac{1}{30}$mol,原混合物中钠与过氧化钠的物质的量之比为:$\frac{1}{6}$mol:$\frac{1}{30}$mol=5:1,故B正确;
故选BD.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握讨论法在化学计算中的应用方法,试题培养了学生的分析、理解能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物.工业上可用CO和H2制取甲醇,化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H=b kJ/mol,
甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物.工业上可用CO和H2制取甲醇,化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H=b kJ/mol,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
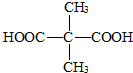 .
.
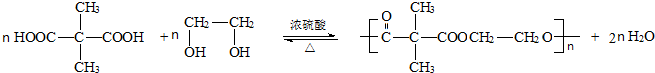 反应类型:缩聚反应.
反应类型:缩聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为NaCl和酚酞和混合溶液浸湿的滤纸,离子交换膜只允许Na+通过,电池充电、放电的化学方程式为2Na2S2+NaBr3$\frac{\underline{\;放电\;}}{充电}$Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )
如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为NaCl和酚酞和混合溶液浸湿的滤纸,离子交换膜只允许Na+通过,电池充电、放电的化学方程式为2Na2S2+NaBr3$\frac{\underline{\;放电\;}}{充电}$Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )| A. | 电池充电时,电极B连接直流电源的正极 | |
| B. | 电池放电过程中Na+从左到右通过离子交换膜 | |
| C. | 闭合开关K后,b电极附近pH变小 | |
| D. | 当b电极上析出气体1120mL(标准状况)时,有0.1 molNa+通过离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 置换反应一定是氧化还原反应 | B. | 化合反应一定是氧化还原反应 | ||
| C. | 中和反应一定是氧化还原反应 | D. | 复分解反应一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2++SO42-═BaSO4↓ | |
| B. | 2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| C. | Al3++2SO42-+2Ba2++3OH-═2BaSO4↓+Al(OH)3↓ | |
| D. | Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com