
【题目】已知Cl﹣、Br﹣、Fe2+、I﹣的还原性依次增强.现向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,请回答: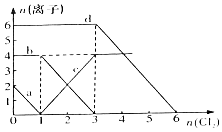
(1)a、c线分别代表溶液中、(填离子符号,下同)的变化情况.
(2)原溶液中Fe2+与Br﹣的物质的量为 .
(3)原混合溶液中FeI2的物质的量为 .
(4)当通入2mol Cl2时,溶液中离子反应为 .
【答案】
(1)I﹣,Fe3+
(2)4mol、6mol
(3)1mol
(4)2Fe2++2I﹣+2Cl2=2Fe3++I2+4Cl﹣
【解析】解:(1)根据还原性强弱为:I﹣>Fe2+>Br﹣>Cl﹣,氧化剂先氧化还原性强的离子,再氧化还原性弱的离子,通入氯气后,碘离子先被氧化,其次是亚铁离子,最后是溴离子,在通入氯气的量为0~1mol的过程中,碘离子从最大量降到0,所以a线代表溶液中的I﹣;
通入氯气的量为1~3mol的过程中,亚铁离子从4mol降到0,三价铁的量逐渐增大,所以c线代表溶液中的Fe3+,
所以答案是:I﹣;Fe3+;
(2)通入氯气的量为1~3mol的过程中,亚铁离子从4mol降到0,三价铁的量逐渐增大,所以含有亚铁离子共4mol,
在通入氯气的量为3~6mol的过程中,溴离子从6mL降到0,所以溴离子的物质的量是6mol,
所以答案是:4mol、6mol;
(3)在通入氯气的量为0~1mol的过程中,碘离子从最大量降到0,即得到碘离子的物质的量为2mol,所以FeI2的物质的量为1mol,
所以答案是:1mol;
(4)当通入2molCl2时,2mol的I﹣消耗氯气1mol,余下的1mol氯气再与2molFe2+反应,即溶液中发生的离子反应可表示为:2Fe2++2I﹣+2Cl2=2Fe3++I2+4Cl﹣;
所以答案是:2Fe2++2I﹣+2Cl2=2Fe3++I2+4Cl﹣.


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.分子间作用力越大,分子越稳定
B.分子间作用力越大,物质的熔、沸点越高
C.相对分子质量越大,其分子间作用力越大
D.分子间只存在范德华力,不存在化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)CO2(g)+H2(g)△H>0
试回答下列问题:
(1)请写出该化学反应的平衡常数表达式: .
(2)830K温度下,若起始时c(CO)=2molL﹣1 , c(H2O)=3molL﹣1 , 达到平衡时CO的转化率为50%,则在该温度下,该反应的平衡常数K= .
(3)若降低温度,该反应的K值将 , 该反应的正反应速率将; 该反应的逆反应速率将(均填“增大”“减小”或“不变”).
(4)若要提高CO的转化率,可采取的措施有: .
(5)830K温度下,若起始时c(CO)=1molL﹣1 , c(H2O)=2molL﹣1 , 反应进行一段时间后,测得H2的浓度为0.5molL﹣1 , 则此时该反应是否达到平衡状态(填“是”与“否”),你判断的依据是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关乙炔分子中的化学键描述不正确的是( )
A.两个碳原子采用sp杂化方式
B.两个碳原子采用sp2杂化方式
C.每个碳原子都有两个未杂化的2p轨道形成π键
D.两个碳原子形成两个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是( ) 
A.若A为浓盐酸,B为MnO2 , C中盛品红溶液,则C中溶液不褪色
B.若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色
D.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是( )
A.等量的硫蒸气和硫固体在氧气中分别完全燃烧,放出热量一样多
B.需要加热才能发生的反应一定是吸热反应
C.在101kpa时,2gH2完全燃烧,生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=﹣285.8kJ/mol
D.在强酸强碱稀溶液中:H+(aq)+OH﹣(aq)=H2O(l)△H=﹣57.3kJ/mol,若将含1molNaOH的溶液和含0.5molH2SO4的浓硫酸混合,放出的热量大于57.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活密切相关,下列有关说法中不正确的是( )
A.工业上可利用铝热反应冶炼金属或焊接钢轨B.84 消毒液与洁厕灵混合使用易产生有毒气体
C.为增强洗涤效果可用热的纯碱溶液洗涤餐具上的油污D.硅胶、六水氯化钙都是常用的食品干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1molL﹣1的是( )
A.将40 g NaOH溶于1 L水所得的溶液
B.将22.4 L HCl溶于水配成1 L溶液
C.1 L含2 mol K+的K2SO4溶液
D.将0.5 molL﹣1的NaNO3溶液100 mL加热蒸发掉50 g 水后的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com