
| 200×(1-81.8%) |
| 16 |
 ,E→F发生消去反应,所以F为
,E→F发生消去反应,所以F为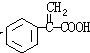 ,F与乙醇发生酯化反应生成G,则G为
,F与乙醇发生酯化反应生成G,则G为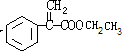 ,G和X互为同分异构体,且具有相同的官能团,则X为
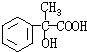
,G和X互为同分异构体,且具有相同的官能团,则X为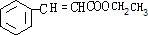 ,Y为
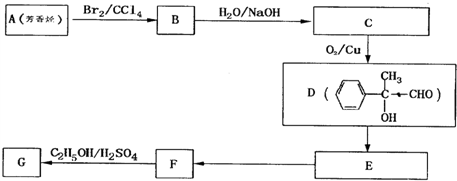
,Y为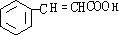 ,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为
,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为 ,据此分析解答.
,据此分析解答.| 200×(1-81.8%) |
| 16 |
 ,E→F发生消去反应,所以F为
,E→F发生消去反应,所以F为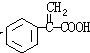 ,F与乙醇发生酯化反应生成G,则G为
,F与乙醇发生酯化反应生成G,则G为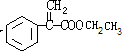 ,G和X互为同分异构体,且具有相同的官能团,则X为
,G和X互为同分异构体,且具有相同的官能团,则X为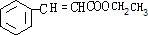 ,Y为
,Y为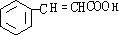 ,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为
,再结合合成路线可知,A→B发生加成,B→C发生水解,C→D发生催化氧化,则A为 ,
,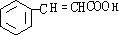 ,Y中含有两个O原子,故答案为:2;
,Y中含有两个O原子,故答案为:2;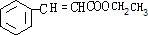 ,其分子式为C11H12O2,故答案为:C11H12O2;
,其分子式为C11H12O2,故答案为:C11H12O2;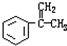 ,故答案为:
,故答案为: ;
;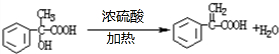 ,故答案为:消去;
,故答案为:消去; ;
;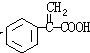 ,F的同分异构体符合下列条件:
,F的同分异构体符合下列条件: ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
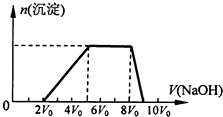 某混合溶液中可能含有的离子如表所示:
某混合溶液中可能含有的离子如表所示:| 可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
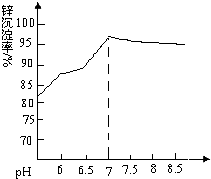 纳米氧化锌是一种新型高功能精细无机产品,由粗氧化锌(含杂质Al2O3、FeO、Fe2O3、CuO等)制备纳米氧化锌.流程依次涉及的部分离子方程式:①FeO+2H+=Fe2++H2O ②H2O2+2Fe2++2H+=2Fe3++2H2O ③Zn+Cu2+=Zn2++Cu
纳米氧化锌是一种新型高功能精细无机产品,由粗氧化锌(含杂质Al2O3、FeO、Fe2O3、CuO等)制备纳米氧化锌.流程依次涉及的部分离子方程式:①FeO+2H+=Fe2++H2O ②H2O2+2Fe2++2H+=2Fe3++2H2O ③Zn+Cu2+=Zn2++Cu| 待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ | Al3+ |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 | 3.7 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 | 4.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如下图所示:
化合物A相对分子质量为86,碳的质量分数为55.8%,氢为7.0%,其余为氧.A的相关反应如下图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com