
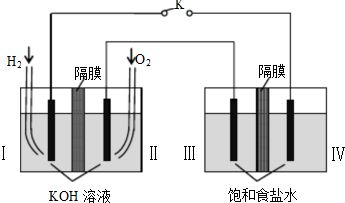
| A、电子流动方向:电极Ⅳ-Ⅰ |
| B、电极Ⅱ电极反应式:O2+2H2O+4e-=4OH- |
| C、电极Ⅲ发生还原反应 |
| D、电极Ⅳ附近观察到黄绿色气体 |


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.4% | B、0.8% |
| C、2% | D、4% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 离子或分子 | 要求 |
| A | Na+、Cl-、CO32-、HCO3- | c(Na+)<c(CO32-) |
| B | Fe3+、SO42-、Cl-、CH3COO- | pH=2 |
| C | Al3+、MnO4-、K+、Cl- | 滴加氨水迅速产生沉淀 |
| D | CH3COOH、NO3-、NH4+、Cu2+ | 添加NaOH 溶液立即产生气泡 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将浓氨水缓慢滴入Al2(SO4)3溶液时候,观察Al(OH)3沉淀的生成和溶解 |
| B、将Al(OH)3浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| C、将Al(OH)3沉淀转入蒸发皿中,加热至无水蒸气逸出,得氧化铝固体 |
| D、分别向Al(OH)3沉淀中加入稀硫酸和NaOH溶液,探究Al(OH)3的两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)>c(F-) |
| B、c(H+)>c(HF) |
| C、c(HF)>c(OH-) |
| D、c(HF)>c(F-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com