
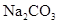 溶液中,下列等量关系成立的是( )
溶液中,下列等量关系成立的是( )| A.c(OH-)= c(H+)+c(HCO3-)+2c(H2CO3) |
| B.2c(Na+)= c(CO32-)+ c(HCO3-)+ c(H2CO3) |
| C.c(Na+)+ c(H+)= c(HCO3-) +2c(CO32-)+ c(OH-) |
| D.c(Na+)="2" c(CO32-)+ c(HCO3-)+ c(H2CO3) |
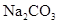 溶液中,根据电荷守恒,可得到c(Na+)+ c(H+)= c(HCO3-) +2c(CO32-)+ c(OH-),故C正确,根据物料守恒,可得到c(Na+)="2" c(CO32-)+2 c(HCO3-)+ 2c(H2CO3),所以BD错误,将c(Na+)="2" c(CO32-)+2 c(HCO3-)+ 2c(H2CO3)代入c(Na+)+ c(H+)= c(HCO3-) +2c(CO32-)+ c(OH-),整理可以得到c(H+)+ 2c(H2CO3) + c(HCO3-)= c(OH-),故A也正确,所以答案为AC。
溶液中,根据电荷守恒,可得到c(Na+)+ c(H+)= c(HCO3-) +2c(CO32-)+ c(OH-),故C正确,根据物料守恒,可得到c(Na+)="2" c(CO32-)+2 c(HCO3-)+ 2c(H2CO3),所以BD错误,将c(Na+)="2" c(CO32-)+2 c(HCO3-)+ 2c(H2CO3)代入c(Na+)+ c(H+)= c(HCO3-) +2c(CO32-)+ c(OH-),整理可以得到c(H+)+ 2c(H2CO3) + c(HCO3-)= c(OH-),故A也正确,所以答案为AC。

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,将pH=3的醋酸溶液加水稀释到原体积的10倍后,溶液的pH=4 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 |
| D.向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+) = c(Cl-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.01 mol·L-1 | B.0.017 mol·L-1 | C.0.05 mol·L-1 | D.0.50 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)= c(NH4+) |
| B.pH = 3的醋酸溶液,稀释至10倍后pH = 4 |
| C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液pH<7 |
| D.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-) 减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 、在此温度下,将pH =8的Ba(OH)2溶液与 PH=5的稀盐酸混合。欲使混合溶液的pH =7,则氢氧化钡溶液与盐酸的体积比为
、在此温度下,将pH =8的Ba(OH)2溶液与 PH=5的稀盐酸混合。欲使混合溶液的pH =7,则氢氧化钡溶液与盐酸的体积比为| A.11:1 | B.9: 2 | C.1:11 | D.2:9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=3的盐酸中,其c(H+)是pH=1的盐酸中的3倍 |
| B.1mol/L0.5L的 AlCl3溶液中,阳离子的物质的量大于0.5mol |
| C.同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的 pH 比 NaCN 溶液大 |
| D.在由水电离出的c(H+) = 1×10-12mol/L的溶液中,K+、ClO-、SO42-一定能大量共存 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a>b | B.a<b | C.a=b | D.无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com