

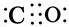 (或C
(或C O) sp3 三角锥形
O) sp3 三角锥形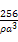
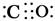 (或C
(或C O);NH3分子中中心原子N的杂化方式为sp3杂化,空间构型为三角锥形。(2)a图中1个黑球周围有6个相邻白球,1个白球周围有3个相邻黑球,故黑∶白=1∶2;b图中1个黑球周围有6个相邻白球,1个白球周围有2个相邻黑球,故黑∶白=1∶3。(3)一个铜晶胞所含有的铜原子数为
O);NH3分子中中心原子N的杂化方式为sp3杂化,空间构型为三角锥形。(2)a图中1个黑球周围有6个相邻白球,1个白球周围有3个相邻黑球,故黑∶白=1∶2;b图中1个黑球周围有6个相邻白球,1个白球周围有2个相邻黑球,故黑∶白=1∶3。(3)一个铜晶胞所含有的铜原子数为 ×8+
×8+ ×6=4,由ρ g/cm3=
×6=4,由ρ g/cm3=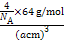 得:NA=
得:NA=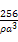 mol-1。
mol-1。

科目:高中化学 来源:不详 题型:填空题
| | CH4 | SiH4 | NH3 | PH3 |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1 073 | 713.2 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | 0.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
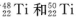 两种原子,它们互称为____。元素在元素周期表中的位置是第_____周期,第____族;基态原子的电子排布式为_____;按电子排布Ti元素在元素周期表分区中属于_____区元素。
两种原子,它们互称为____。元素在元素周期表中的位置是第_____周期,第____族;基态原子的电子排布式为_____;按电子排布Ti元素在元素周期表分区中属于_____区元素。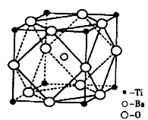
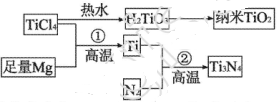 。
。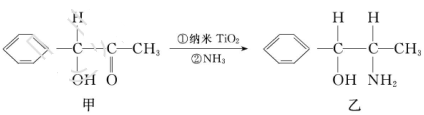
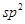 杂化的碳原子个数为_____,化合物乙中采取
杂化的碳原子个数为_____,化合物乙中采取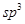 杂化的原子的第一电离能由大到小的顺序为_____。
杂化的原子的第一电离能由大到小的顺序为_____。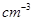 (NA为阿伏加德罗常数的数值,只列算式)。
(NA为阿伏加德罗常数的数值,只列算式)。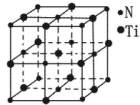
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| Q | Q的单质是实验室常用的惰性电极材料 |
| R | R原子基态时2p原子轨道上有3个未成对电子 |
| T | 负二价的元素T的氢化物在通常状况下是一种液体,且其中T的质量分数为88.9% |
| X | X是第三周期电负性最大的元素 |
| Y | 元素Y位于周期表的第10列 |
| Z | Z存在质量数为65,中子数为36的核素 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 738 | 1 451 | 7 733 | 10 540 |
 ),下列说法正确的是________(填序号)。
),下列说法正确的是________(填序号)。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com