
| A. | 已知S(g)+O2(g)═SO2(g)△H1;S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 | |
| B. | HCl和NaOH反应的中和热△H=-57.3kJ•mol-1,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ•mol-1 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 氢气的燃烧热为285.5 kJ•mol-1,则水分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 |
分析 A.固体硫燃烧时要先变为气态硫,过程吸热,据此确定反应热的大小;
B.中和热是指在稀溶液中,强酸和强碱反应生成1mol水时放出的热量;
C.物质具有能量越高,物质稳定性越差;
D.2mol氢气燃烧生成液态水放出热量为571kJ,则2mol液态水分解吸热热量为571kJ.
解答 解:A.固体硫燃烧时要先变为气态硫,过程吸热,气体与气体反应生成气体比固体和气体反应生成气体产生热量多,但反应热为负值,所以△H1<△H2,故A正确;
B.中和热是指在稀溶液中,强酸和强碱反应生成1mol水时放出的热量,其衡量标准是生成的水为1mol,故无论稀H2SO4和Ba(OH)2反应生成的水是几摩尔,中和热为生成1mol水放出的热量,故B错误;
C.已知C(石墨,s)=C(金刚石,s)△H>0,该反应为吸热反应,则石墨具有的能量小于金刚石,则石墨比金刚石稳定,故C错误;
D.氢气的燃烧热为285.5 kJ•mol-1,则2mol液态水分解吸热热量为571kJ,正确的热化学方程式为:2H2O(l)═2H2(g)+O2(g)△H=+571 kJ•mol-1,故D错误;
故选A.
点评 本题综合考查了热化学方程式,涉及热化学方程式书写、中和热、物质稳定性等知识,为高频考点,题目难度不大,侧重于基本概念的综合理解和运用的考查,注意相关基础知识的积累.


科目:高中化学 来源: 题型:实验题
 如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:
如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
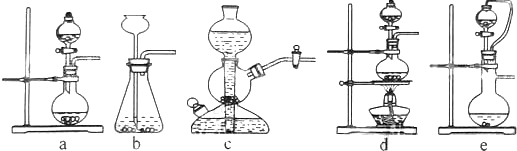
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl、CuCl2、Ba(OH)2 | B. | NaOH、CuSO4、H2SO4 | ||
| C. | Ba(OH)2、H2SO4、K2SO4 | D. | NaBr、H2SO4、Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
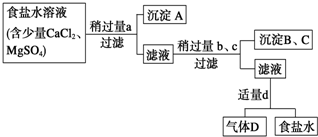

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com