
 2SO3(g) +Q
2SO3(g) +Q
| A£®Ķ¼Ņ»ŃŠ¾æµÄŹĒĪĀ¶Č”¢Ń¹Ēæ¶ŌĘ½ŗāµÄÓ°Ļģ£¬ŗį×ų±ź±ķŹ¾Ń¹Ēæ |
| B£®Ķ¼¶žŃŠ¾æµÄŹĒĪĀ¶Č¶ŌĘ½ŗāµÄÓ°Ļģ£¬¢ņ²ÉÓƵÄĪĀ¶Čøüøß |
| C£®Ķ¼ČżÖŠt0Ź±Ź¹ÓĆĮĖ“߻ƼĮ£¬Ź¹Ę½ŗāĻņÕż·“Ó¦·½Ļņ½ųŠŠ |
| D£®Ķ¼ĖÄÖŠt0Ź±Ōö“óŃ¹Ē棬Ź¹Ę½ŗāĻņÕż·“Ó¦·½Ļņ½ųŠŠ |
 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 2NO2(g)µÄĘ½ŗā”£ĻĀĶ¼±ķŹ¾²ā¶ØN2O4µÄÅضČÓėŹ±¼ä¹ŲĻµµÄĒśĻߣØׯ×ų±źĪŖN2O4µÄÅØ¶Č£¬ŗį×ų±źĪŖŹ±¼ä£©”£
2NO2(g)µÄĘ½ŗā”£ĻĀĶ¼±ķŹ¾²ā¶ØN2O4µÄÅضČÓėŹ±¼ä¹ŲĻµµÄĒśĻߣØׯ×ų±źĪŖN2O4µÄÅØ¶Č£¬ŗį×ų±źĪŖŹ±¼ä£©”£
|
| T/K | 310 | 320 |
| KÖµ | 0.38 | 0.42 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 CO2£Øg£©+H2£Øg£©“ļµ½Ę½ŗāדĢ¬£¬Õż·“Ó¦ĖŁĀŹĖꏱ¼ä±ä»ÆµÄŹ¾ŅāĶ¼ČēĻĀĖłŹ¾”£ÓÉĶ¼æÉµĆ³öµÄÕżČ·½įĀŪŹĒ
CO2£Øg£©+H2£Øg£©“ļµ½Ę½ŗāדĢ¬£¬Õż·“Ó¦ĖŁĀŹĖꏱ¼ä±ä»ÆµÄŹ¾ŅāĶ¼ČēĻĀĖłŹ¾”£ÓÉĶ¼æÉµĆ³öµÄÕżČ·½įĀŪŹĒ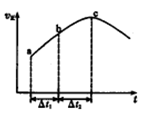
| A£®·“Ó¦ĪļÅØ¶Č£ŗaµćŠ”ÓŚcµć |
| B£®cµćŹ±·“Ó¦½ųŠŠµÄ³Ģ¶Č×ī“ó |
| C£®øĆ·“Ó¦µÄÕż·“Ó¦ĪŖĪüČČ·“Ó¦ |
| D£®”÷t1=”÷t2Ź±£¬Éś³ÉH2µÄĪļÖŹµÄĮæ£ŗa~b¶ĪŠ”ÓŚb~c¶Ī |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 4NO(g)+6H2O(g)¦¤H=-akJ/mol(a©0)
4NO(g)+6H2O(g)¦¤H=-akJ/mol(a©0)
| ÅضČ(mol/L) Ź±¼ä(min) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| Ęš Ź¼ | 4.0 | 5.5 | 0 | 0 |
| µŚ2min | 3.2 | x | 0.8 | 1.2 |
| µŚ4min | 2.0 | 3.0 | 2.0 | 3.0 |
| µŚ6min | 2.0 | 3.0 | 2.0 | 3.0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 2Cl2+2H2O£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ”£
2Cl2+2H2O£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 CO(g)+H2(g)?131.4 kJӣ
CO(g)+H2(g)?131.4 kJӣ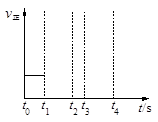
 CH3OH(g) ¢ŚCO(g) + CH3OH(g)
CH3OH(g) ¢ŚCO(g) + CH3OH(g) HCOOCH3(g)
HCOOCH3(g)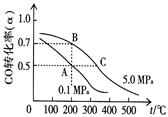
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 2Z(g) ”÷H£¼
2Z(g) ”÷H£¼ £¬ČēĶ¼ŹĒ·“Ó¦“ļĘ½ŗā¼°øıäĢõ¼žĘ½ŗāŅĘ¶ÆµÄĶ¼Ļń”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
£¬ČēĶ¼ŹĒ·“Ó¦“ļĘ½ŗā¼°øıäĢõ¼žĘ½ŗāŅĘ¶ÆµÄĶ¼Ļń”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ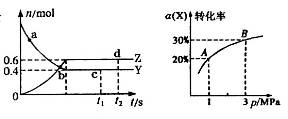
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 2NH3(g) ”÷H£¼0µÄÄ£ÄāŃŠ¾æ£¬ŌŚ1LĆܱÕČŻĘ÷ÖŠ£¬·Ö±š¼ÓČė0.1mol N2ŗĶ0.3mol H2”£ŹµŃé¢Ł”¢¢Ś”¢¢ŪÖŠc£ØN2£©Ėꏱ¼ä£Øt£©µÄ±ä»ÆČēĶ¼ĖłŹ¾”£
2NH3(g) ”÷H£¼0µÄÄ£ÄāŃŠ¾æ£¬ŌŚ1LĆܱÕČŻĘ÷ÖŠ£¬·Ö±š¼ÓČė0.1mol N2ŗĶ0.3mol H2”£ŹµŃé¢Ł”¢¢Ś”¢¢ŪÖŠc£ØN2£©Ėꏱ¼ä£Øt£©µÄ±ä»ÆČēĶ¼ĖłŹ¾”£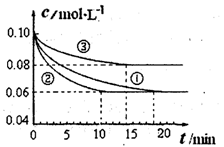
 2N2(g)£«3H2O(g) ”÷H£¼0ÓūĢįøß·ĻĘųÖŠµŖŃõ»ÆĪļµÄ×Ŗ»ÆĀŹ£¬æɲÉČ”µÄ“ėŹ©ŹĒ £ØĢī×ÖÄø£©
2N2(g)£«3H2O(g) ”÷H£¼0ÓūĢįøß·ĻĘųÖŠµŖŃõ»ÆĪļµÄ×Ŗ»ÆĀŹ£¬æɲÉČ”µÄ“ėŹ©ŹĒ £ØĢī×ÖÄø£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÅØ¶Č | B£®Ń¹Ēæ | C£®ĪĀ¶Č | D£®“߻ƼĮ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com