
【题目】用钌(Ru)基催化剂催化CO2(g)和H2(g)的反应时,每生成92g液态HCOOH放出62.4kJ的热量,下列说法正确的是( )
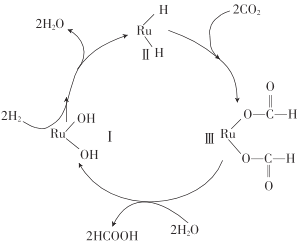
A.图示中物质II为该反应的催化剂
B.图示中参与循环的物质只有CO2和H2
C.反应的活化能为62.4kJ·mol-1
D.该反应的热化学方程式为H2(g)+CO2(g)=HCOOH(l) △H=-31.2kJ·mol-1
【答案】D
【解析】
根据图示,发生反应CO2+H2=HCOOH,氢气和物质Ⅰ作用生成水,CO2与物质Ⅱ作用生成物质Ⅲ,物质Ⅲ和水反应生成甲酸和物质Ⅰ。可知反应物是H2和CO2,催化剂为物质Ⅰ,其他为中间产物。
A.根据分析物质Ⅰ是催化剂,而物质Ⅱ是H2与催化剂反应生成的中间产物,A错误;
B.参与循环的物质除了CO2、H2,还有H2O,B错误;
C.该反应每生成92g液体HCOOH,即2molHCOOH,放出热量62.4kJ,而不是该反应的活化能是62.4kJ·mol-1,C错误;
D.该反应每生成92g液体HCOOH,即2molHCOOH,放出热量62.4kJ,可写出热化学方程式为H2(g)+CO2(g)=HCOOH(l) △H=-31.2kJ·mol-1,D正确。
答案选D。


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】以A、B、C为原料制取药物AspirinSustained-ReleaseTablets(缓释阿司匹林)的合成路线如图:

已知:ⅰ.A、B为烃,其中A的产量可作为石油化工水平的标志;
ⅱ. 。
。
回答下列问题:
(1)Z所含官能团名称为___。
(2)B和Y的结构简式为__、__。
(3)完成方程式:
①X→CH2OHCH2OH__。
②C→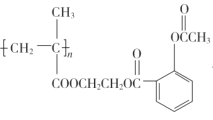 __。
__。
(4)满足以下条件的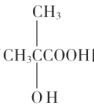 的同分异构体共有__种(不含立体异构),其中核磁共振氢谱峰面积比为6:1:1的同分异构体的结构简式为__。
的同分异构体共有__种(不含立体异构),其中核磁共振氢谱峰面积比为6:1:1的同分异构体的结构简式为__。
a.能发生水解反应 b.能与钠反应放出氢气 c.能发生银镜反应
(5)以乳酸(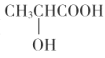 )和甲醇为原料,其他无机试剂任选,设计合成
)和甲醇为原料,其他无机试剂任选,设计合成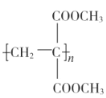 的路线:__。
的路线:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体。下列说法错误的是( )

A. S2Cl2的结构式为Cl-S-S-Cl
B. S2Cl2为含有极性键和非极性键的非极性分子
C. S2Br2与S2Cl2结构相似,分子间作用力:S2Br2>S2Cl2
D. S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁氮化合物(![]() )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某![]() 的制备需铁、氮气、丙酮和乙醇参与。
的制备需铁、氮气、丙酮和乙醇参与。
(1)![]() 基态核外电子排布式为_______。
基态核外电子排布式为_______。
(2)丙酮(![]() )分子中碳原子轨道的杂化类型是_______,1mol丙酮分子中含有σ键的数目为______________。
)分子中碳原子轨道的杂化类型是_______,1mol丙酮分子中含有σ键的数目为______________。
(3)C、H、O三种元素的电负性由小到大的顺序为_____。
(4)乙醇的沸点高于丙酮,这是因为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4(阱)可作制药的原料,也可作火箭的燃料。已知热化学方程式:
反应I:N2H4(g)![]() N2(g)+2H2(g) △H1>0;
N2(g)+2H2(g) △H1>0;
反应II:N2(g)+3H2(g)![]() 2NH3(g) △H2<0;
2NH3(g) △H2<0;
反应III:N2H4(g)+H2(g)![]() 2NH3(g) △H。
2NH3(g) △H。
下列推断不正确的是( )
A.N2H4断裂共价键需要吸收能量
B.反应I中1molN2H4(g)的能量小于1molN2(g)和2molH2(g)的总能量
C.反应II中正反应的活化能大于逆反应的活化能
D.△H=△H1+△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列说法错误的是
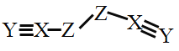
A.化合物WY是良好的耐热冲击材料
B.Y的氧化物对应的水化物可能是弱酸
C.X的氢化物的沸点一定小于Z的
D.化合物(ZXY)2中所有原子均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年国际非政府组织“全球碳计划”12月4日发布报告:研究显示,全球二氧化碳排放量增速趋于缓。CO2的综合利用是解决温室问题的有效途径。
(1)一种途径是将CO2转化为成为有机物实现碳循环。如:
C2H4 (g) + H2O (l) = C2H5OH (l) ΔH=-44.2 kJ·mol-1
2CO2(g) + 2H2O (l) =C2H4 (g) +3O2(g) ΔH=+1411.0 kJ·mol-1
2CO2(g) + 3H2O (l) = C2H5OH (l) + 3O2(g) ΔH=___________
(2)CO2甲烷化反应是由法国化学家Paul Sabatier 提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程:
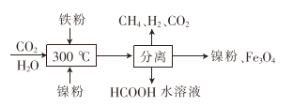
①上述过程中,产生H2反应的化学方程式为:___________________________________。
②HCOOH是CO2转化为CH4的中间体:CO2 ![]() HCOOH
HCOOH ![]() CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉的用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是_______________(填I或II)
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉的用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是_______________(填I或II)
(3)CO2经催化加氢可以生成低碳烃,主要有两个竞争反应:
反应I:CO2(g) + 4H2 (g)![]() CH4 (g) +2H2O(g)
CH4 (g) +2H2O(g)
反应II:2CO2(g) + 6H2 (g)![]() C2H4 (g) +4H2O(g)
C2H4 (g) +4H2O(g)
在1L密闭容器中冲入1molCO2和4molH2,测得平衡时有关物质的物质的量随温度变化如图所示。T1℃时,CO2的转化率为_________。T1℃时,反应I的平衡常数K=_______。

(4)已知CO2催化加氢合成乙醇的反应原理为2CO2(g) + 6H2 (g)![]() C2H5OH (g) +4H2O(g) ΔH,m代表起始时的投料比,即m=
C2H5OH (g) +4H2O(g) ΔH,m代表起始时的投料比,即m=![]() .
.
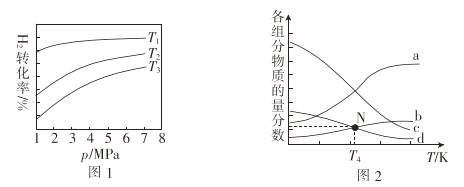
①图1中投料比相同,温度T3>T2>T1,则ΔH_____(填“>”或“<”)0.
②m=3时,该反应达到平衡状态后p(总)=20ɑ MPa ,恒压条件下各物质的物质的量分数与温度的关系如图2.则曲线b代表的物质为_______(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铜阳极泥(主要成分是Cu2Te,含Ag、Au等杂质)为原料提取碲并回收金属,其工艺流程如下:
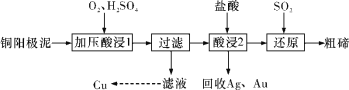
已知:TeO2是两性氧化物,微溶于水,易溶于较浓的强酸和强碱。下列说法错误的是
A.“加压酸浸1”过程中将碲元素转化成TeO2,应严格控制溶液的pH值
B.“酸浸2”过程中温度不能过高,否则会使碲的浸出率降低
C.从Ag和Au中分离出Au,应该向回收的Ag和Au中加入稀氨水
D.“还原”反应中发生的离子方程式为:TeO2+2SO2+2H2O=Te+2SO42-+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,H2CO3的Ka1=4.2×10-7,Ka2=5.0×10-11。常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入40mL0.1mol/L'HCl溶液,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
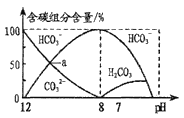
下列说法正确的是
A. 在同一溶液中,H2CO3、HCO3-、CO32-能大量共存
B. a点时:c(Na+)+c(H+)=c(OH-)+3c(CO32-)
C. 当pH=7时,溶液中c(Na+)=c(HCO3-)+2c(CO32-)
D. 当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com