
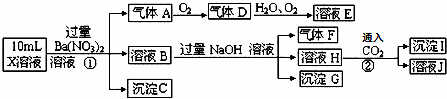
某强酸性溶液X中可能含有Fe2+、A13+、NH4+、CO32﹣、SO32﹣、SO42﹣、C1﹣中的若干种,现取X溶液进行连续实验,实验过程及产物如图.下列说法正确的是()
A. 气体A是NO2
B. X中肯定存在Fe2+、A13+、NH4+、SO42﹣
C. 溶液E和气体F不能发生化学反应
D. X中不能确定的离子是 A13+和C1﹣
考点: 常见离子的检验方法.
专题: 离子反应专题.
分析: 强酸性溶液,一定没有CO32﹣、SO32﹣;加入硝酸钡,引进硝酸根,溶液具有强氧化性,一定含有亚铁离子,故A是一氧化氮,D是二氧化氮,E是硝酸;沉淀C是硫酸钡,溶液中一定含有硫酸根;加入过量氢氧化钠,产生的气体F是氨气,溶液中一定含有铵离子,生成了沉淀G;H中通入二氧化碳,生成沉淀I,沉淀可能为氢氧化铝或碳酸钡;根据以上分析,对选项逐一判断.
解答: 解:X是强酸性溶液,一定不会含有弱酸根离子:CO32﹣、SO32﹣;
加入硝酸钡,溶液具有了强氧化性,故气体A是一氧化氮,D是二氧化氮,E则为硝酸,故溶液中一定含有还原性的离子:Fe2+;
B中加入氢氧化钠产生了气体F,F一定是氨气,溶液中一定含有铵离子;
H中通入二氧化碳生成了沉淀I,I可能为氢氧化铝或在碳酸钡,故溶液中不一定含有铝离子;
沉淀C为硫酸钡,溶液中一定含有硫酸根;
A、气体A是一氧化氮,故A错误;
B、根据分析,X中肯定存在Fe2+、NH4+、SO42﹣,不能确定是否含有铝离子,故B错误;
C、E是硝酸,F是氨气,可以发生反应,故C错误;
D、根据分析可知,溶液中可能含有铝离子和氯离子,故D正确;
故选D.
点评: 本题考查常见离子的检验,如氨气的检验、铝离子的检验等,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2O4+8H2O 3Zn(OH)2+2Fe(OH)3+2Fe(OH)3+4KOH下列叙述不正确的是()
3Zn(OH)2+2Fe(OH)3+2Fe(OH)3+4KOH下列叙述不正确的是()
A. 放电时负极反应为:3Zn﹣6e﹣+6OH﹣═3Zn(OH)2
B. 放电时正极反应为:2FeO42﹣+6e﹣+8H2O═2Fe(OH)3+10OH﹣
C. 放电时每转移3mol电子,正极有1mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
某盐的溶液中含有Na+、Mg2+、Cl﹣、SO42﹣四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl﹣为0.4mol,则SO42﹣物质的量为()
A. 0.1mol B. 0.3mol C. 0.5mol D. 0.15mol
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中少量杂质的方法不正确的是()
A. 除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
B. 除去CO2中混有的HCl:用饱和NaHCO3溶液洗气
C. 除去BaCO3固体中混有的BaSO4:加入过量的盐酸、过滤、洗涤
D. 除去甲烷中混有的乙炔:通过溴水溶液后,洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
在反应3Cl2+8NH3→6NH4Cl+N2中,设阿伏加德罗常数为NA.则下列说法正确的是()
A. 若有0.3 mol Cl2参加反应,转移的电子数为0.6NA
B. 若生成2.24 L氮气,转移的电子数为0.6NA
C. 若有1.2NA个电子发生转移,则被氧化的氨气的质量是27.2 g
D. 若生成1 mol的氯化铵转移电子数是n个,则NA=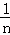
查看答案和解析>>
科目:高中化学 来源: 题型:
焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈.发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe 和X.
(1)根据题意,可判断出X是 (写化学式).
(2)写出并配平该反应的化学方程式:
(3)发生氧化反应的物质是 ,反应中4mol的氧化剂能 (填“失去”或“得到”) mol电子.
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数),下列说法正确的是()
A. 若X(OH)n为强碱,则Y(OH)n也一定为强碱
B. 若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C. 若X形成的单质是X 2,则Y元素形成的单质一定是Y2
2,则Y元素形成的单质一定是Y2
D. 若Y的最高正价为+m,则X的最高正价一定为+m
查看答案和解析>>
科目:高中化学 来源: 题型:
如表为元素周期表中的一部分.用化学式或元素符号回答下列问题:
IA ⅡA ⅢA IVA VA ⅥA VⅡA 0
2 ⑥ ⑦
3 ① ③ ⑤ ⑧ ⑩
4 ② ④ ⑨
(1)10种元素中,化学性质最不活泼的是氩(填元素名称).
(2)在①②⑤的最高价氧化物的水化物中,碱性最强的是 (填化学式).
(3)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(4)⑧与⑨分别与H2形成的氢化物的稳定性:HCl HBr,(用化学式表示)最高价氧化物对应的水溶液的酸性 .(用化学式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com