
分析 (1)碳酸钠和盐酸反应生成氯化钠、水以及二氧化碳,碳酸氢钠和盐酸反应生成氯化钠、水以及二氧化碳;
(2)二氧化碳和澄清石灰水反应生成碳酸钙和水,过量的二氧化碳碳酸钙反应生成碳酸氢钙;
(3)为了避免浪费,实验中取的试剂要少量;
(4)碳酸氢钠和盐酸相遇立即反应产生二氧化碳,碳酸钠和盐酸反应生成碳酸氢钠和氯化钠,然后是碳酸氢钠和盐酸反应生成氯化钠、水以及二氧化碳,据此回答.
解答 解:(1)碳酸钠和盐酸反应生成氯化钠、水以及二氧化碳,Na2CO3+2HCl=2NaCl+H2O+CO2↑,碳酸氢钠和盐酸反应生成氯化钠、水以及二氧化碳NaHCO3+HCl=NaCl+H2O+CO2↑,故答案为:NaHCO3+HCl=NaCl+H2O+CO2↑、Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)二氧化碳和澄清石灰水反应先产生白色沉淀,继续通入,白色沉淀消失.发生反应为:CO2+Ca2++2OH-=CaCO3↓+H2O、CaCO3+CO2+H2O=Ca2++2HCO3-,故答案为:CO2+Ca2++2OH-=CaCO3↓+H2O、CaCO3+CO2+H2O=Ca2++2HCO3-;
(3)为了避免浪费,实验中取的试剂要少量,故答案为:取样或取少量样品;
(4)碳酸氢钠和盐酸相遇立即反应产生二氧化碳,碳酸钠和盐酸反应生成碳酸氢钠和氯化钠,然后是碳酸氢钠和盐酸反应生成氯化钠、水以及二氧化碳,验是纯碱还是小苏打,可以将样品各取少量配置成溶液,将稀盐酸滴入其中,开始就能够产生气泡的是碳酸氢盐,持续滴入才产生气泡的是碳酸盐,
故答案为:样品各取少量配置成溶液,将稀盐酸滴入其中;开始就能够产生气泡的是碳酸氢盐,持续滴入才产生气泡的是碳酸盐;碳酸氢钠和盐酸相遇立即反应产生二氧化碳,碳酸钠和盐酸反应生成碳酸氢钠和氯化钠,然后是碳酸氢钠和盐酸反应生成氯化钠、水以及二氧化碳.
点评 本题考查学生含碳元素的化合物的性质,注意碳酸钠和碳酸氢钠和盐酸反应的区别是关键,难度中等.


科目:高中化学 来源: 题型:选择题

| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 工业上通过氯碱工业制取金属钠 | |
| C. | 从第③步到第⑤步的目的是浓缩、富集溴单质 | |
| D. | 第②步的反应条件是高温加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用H2表示的反应速率为0.1 mol/(L•min) | |
| B. | 用NH3表示的反应速率为0.3 mol/(L•min) | |
| C. | 用N2表示的反应速率为0.2mol/(L•min) | |
| D. | 用H2表示的反应速率为0.3 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | 只有① | C. | ②④ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
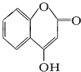 是用来制备抗凝血药的医药中间体,可通过下列路线合成:
是用来制备抗凝血药的医药中间体,可通过下列路线合成:
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二者的分子个数之比为17:16 | B. | 二者的原子个数之比为17:16 | ||
| C. | 二者的氢原子个数之比为17:12 | D. | 在相同条件下二者体积比为17:16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用核磁共振氢谱图可鉴别1-溴丙烷和2-溴丙烷 | |
| B. | 有机物的同系物具有相同的最简式 | |
| C. | 石油和煤都是混合物,但通过化学方法石油分馏出的汽油是纯净物 | |
| D. | 煤中含有煤焦油及多种化工原料,可通过物理方法煤的干馏获得 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com