
下列说法不正确的是
A、在固定体积的密闭容器中发生可逆反应A(s)+B(g)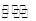 C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态
C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态
B、对于反应C(s)+CO2(g)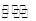 2CO(g) △H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
2CO(g) △H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
C、向0.1mol·L-1的NH3·H2O中加入氯化铵固体,则溶液中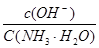 增大
增大
D、常温下向Mg(OH)2悬浊液中加入MgCl2浓溶液后,溶液中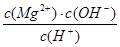 不变
不变
C
【解析】在反应A(s)+B(g) C(g)+D(g)中, A是固体,反应容器体积固定,故达到平衡前气体的密度随气体质量变化而变化,当气体密度不再改变时,说明已达到化学平衡状态,A正确;△H>0,说明反应C(s)+CO2(g)
C(g)+D(g)中, A是固体,反应容器体积固定,故达到平衡前气体的密度随气体质量变化而变化,当气体密度不再改变时,说明已达到化学平衡状态,A正确;△H>0,说明反应C(s)+CO2(g)  2CO(g)是吸热反应,化学平衡常数增大,说明反应温度升高,因而反应速率也一定增大,B正确;氨水中存在电离平衡:NH3·H2O
2CO(g)是吸热反应,化学平衡常数增大,说明反应温度升高,因而反应速率也一定增大,B正确;氨水中存在电离平衡:NH3·H2O NH4++OH- ,加入氯化铵固体后增大了c(NH4+),平衡向左移动,c(OH-)减小而c(NH3·H2O)增大,故
NH4++OH- ,加入氯化铵固体后增大了c(NH4+),平衡向左移动,c(OH-)减小而c(NH3·H2O)增大,故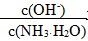
减小,C错误;Mg(OH)2悬浊液中存在着溶解平衡
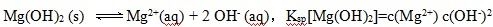
故
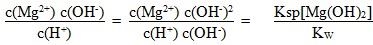 ,
,
而Ksp[Mg(OH)2]与KW均是温度的函数,不随浓度变化而改变,D正确。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源:2014高考名师推荐化学--预测14 题型:选择题
相对分子质量为100的有机物A能与钠反应,且完全燃烧只生成CO2和H2O。若A含一个六碳环,则环上一氯代物的数目为( )
A、5 B、4 C、3 D、2
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测12 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的是
A.7.8 g Na2O2中含有的离子总数目为0.4NA
B.1mol 苯分子中含有碳碳双键数目为3NA
C.标准状况下,将分子总数为NA的NH3和HCl气体混合后的体积约为22. 4L
D.16g CH4与18 g NH4+ 所含电子数均为10NA
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:简答题
【物质结构与性质】
根据元素周期表中第四周期元素的相关知识,回答下列问题:
(1)第四周期元素的基态原子的电子排布中4s轨道上只有1个电子的元素有________种;写出Cu+的核外电子排布式________。
(2)按电子排布,可将周期表里的元素划分成五个区域,第四周期元素中属于s区的元素有________种,属于d区的元素有________种。
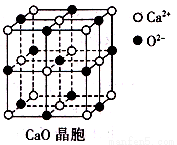
(3)CaO晶胞如所示,CaO晶体中Ca2+的配位数为 ;CaO的焰色反应为砖红色,许多金属或它们的化
合物都可以发生焰色反应,其原因是_______。
(4)由叠氮化钾(KN3)热分解可得纯N2:2KN3(s)=2K(l)+3N2(g),下列有关说法正确的是_______(填选项字母)。
A NaN3与KN3结构类似,前者晶格能较小
B晶体钾的晶胞结构如图所示: ,每个晶胞中分摊2个钾原子
,每个晶胞中分摊2个钾原子
C氮的第一电离能大于氧
D氮气常温下很稳定,是因为氮的电负性小
(5)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂。O2在其催化作用下,可将CN-氧化成CNO-。CN-的电子式为_______,CNO-的中心原子的杂化方式为______。
(6)在CrCl3溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+ (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
[CrCln(H2O)6-n]X++ xR- Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。
Rx[CrCln(H2O)6-n]+xH+。将含0.0015 mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 mL,则该配离子的化学式为_______。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:选择题
下列实验不能达到目的的是
选项 | 实验操作 | 实验目的 |
A | 向5 mL 0.1 mol/L AgNO3溶液中滴加3滴0.1 mol/LNaCl溶液,产生白色沉淀;再向其中滴加3滴0.1mol/L的KI溶液,有黄色沉淀产生 | 验证Ksp(AgCl)> Ksp(AgI) |
B | 向适量样品溶液中滴加KSCN溶液 | 检验FeSO4溶液是否被氧化 |
C | 向适量样品溶液中滴加盐酸酸化,再滴加BaCl2溶液 | 检验Na2SO3溶液是否被氧化 |
D | 向Na2SiO3溶液中通入CO2 | 验证非金属性:碳>硅 |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测10 题型:填空题
一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。工业上依此用CO生产燃料甲醇。
CH3OH(g)。工业上依此用CO生产燃料甲醇。
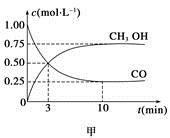
(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(CO)=__________________。
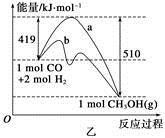
(2)乙图表示该反应进行过程中能量的变化。曲线b下的反应条件为 。该反应的焓变是________(填“ΔH<0”或“ΔH>0”),写出反应的热化学方程式 ;选择适宜的催化剂______(填“能”或“不能”)改变该反应的反应热。
(3)该反应平衡常数K的表达式为______________________,温度升高,平衡常数K________(填“增大”、“不变”或“减小”)。
(4)恒容条件下,下列措施中能使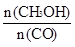 增大的有____________。
增大的有____________。
a.降低温度 b.充入He气
c.再充入1molCO和2molH2 d.使用催化剂
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测10 题型:选择题
下列有关说法正确的是
A.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液
B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解
C.反应N2(g)+3H2(g) 2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大
2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大
D.吸热反应“TiO2(s)+2Cl2(g) TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0
TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测1 题型:简答题
有机物A(C9H10O2)在光照条件下生成的一溴代物B有下列转化关系(无机产略):
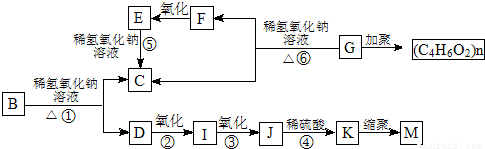
已知:①K的一卤代产物只有两种同分异构体;
②当羟基与双键碳原子相连时,易发生下列转化:RCH=CHOH→RCHCHO
请回答下列问题
(1)G中官能团的名称 ;
(2)上述反应属于取代反应的是 ;
(3)写出与E互为同分异体且含有两种官能团的有机X的结构式 ;
(4)写出反应①的化学方程式: ;
(5)符合下列条件的A的同分异构体有 种;
I含有苯环
II能发生银镜反应和水解反应
III在稀氢氧化钠溶液中,1mol该能与1molNOH反应
请任写出其中的一种同分异构体的结构简式 ;
查看答案和解析>>
科目:高中化学 来源:2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷(解析版) 题型:选择题
(15分) 现有A、B、C、D、E、F、G七种短周期元素,原子序数依次增大。已知A与E、D与F分别同主族, E、F、G同周期;A、C的最外层电子数之和与D的最外层电子数相等,A与D形成的化合物常温下为液态,A分别与F、G形成的气体分子电子总数相等、B有多种同素异形体,其中一种是原子晶体,是自然界中最硬的物质,可做首饰品或做切削工具。
请回答下列问题:
(1)元素C在周期表中的位置是_______________
元素E的原子结构示意图为
(2)C的气态氢化物的水化物与其最高价氧化物的水化物可发生反应,离子方程式为:
(3)在一定条件下,A、D的单质和A、D、E形成的离子化合物的水溶液可构成电池,该电池负极的电极反应式为 , 该电池在放电过程中,电解质溶液的pH将________(填“增大”、“减小”或“不变”)。
(4)化合物C2A4(g) 是一种高效清洁的火箭燃料,0.25 mol C2A4完全燃烧的生成物是一种气态单质和一种气态化合物,它们对环境无污染,同时放出热量133.5 kJ的热量。则该反应的热化学方程式为(用具体物质化学式表示) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com