
ШчЭМБэЪОФГЮТЖШЪБЃЌЗДгІN2O4(g) 2NO2(g)дкЧА110 sФкЕФЗДгІНјааЧщПіЃЌЧыИљОнЭМЯёЛиД№ЯТСаЮЪЬтЁЃ
2NO2(g)дкЧА110 sФкЕФЗДгІНјааЧщПіЃЌЧыИљОнЭМЯёЛиД№ЯТСаЮЪЬтЁЃ

(1)ИУПЩФцЗДгІДяЕНЦНКтЕФЪБМфЖЮЮЊ ЁЃ
(2)ЗДгІНјааЕН70 sЪБЃЌИФБфЕФЬѕМўПЩФмЪЧ (ЬюзжФИЃЌЯТЭЌ),ЗДгІНјааЕН90 sЪБЃЌИФБфЕФЬѕМўПЩФмЪЧ ЁЃ
A.МгШыДпЛЏМС B.РЉДѓШнЦїЬхЛ§
C.Щ§ИпЮТЖШ D.діДѓN2O4ЕФХЈЖШ
(3)90 sКѓШєЮЌГжШнЦїЕФЬхЛ§ВЛБфЃЌЦНКтвЦЖЏЕФЗНЯђЮЊ (ЬюЁАе§ЗДгІЁБЁЂЁАФцЗДгІЁБЛђЁАВЛвЦЖЏЁБ)ЃЌДЫЪБN2O4ЕФзЊЛЏТЪ (ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЁЃ
(4)ЧыдкЭМжаЛГіЗДгІЮяN2O4дк0ЁЋ70УыЪБЕФХЈЖШБфЛЏЧњЯпЁЃ
(1)60ЁЋ70 sЁЂ80ЁЋ90 sЁЂ100ЁЋ110 s (2)B D
(3)е§ЗДгІ МѕаЁ
(4)
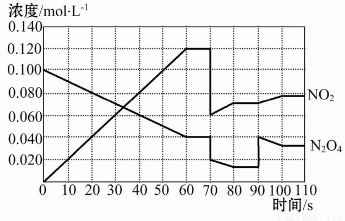
ЁОНтЮіЁП(1)гЩЭМЯёПЩжЊЗДгІДяЕНЦНКтЕФЪБМфЖЮЮЊ60ЁЋ70 sЁЂ80ЁЋ90 sКЭ100ЁЋ110 sЁЃ
(2)ЗДгІНјааЕН70 sЪБИФБфФГвЛЬѕМўЃЌПЩвдПДГіNO2ЕФХЈЖШбИЫйДг0.120 molЁЄL-1МѕаЁЕН0.060 molЁЄL-1ЃЌN2O4ЕФХЈЖШДг0.040 molЁЄL-1МѕаЁЕН0.020 molЁЄL-1ЃЌСНепЕФХЈЖШЖММѕаЁЕНдРДЕФ1/2ЃЌЫЕУїИФБфЕФЬѕМўЮЊдіДѓШнЦїЕФЬхЛ§ЮЊдРДЕФ2БЖЛђМѕаЁбЙЧПЮЊдРДЕФ1/2ЃЛ90 sЪБЭЛШЛИФБфФГвЛЬѕМўПЩвдПДГіNO2ЕФХЈЖШЫВМфУЛгаИФБфЃЌЕЋЪЧN2O4ЕФХЈЖШЫВМфдіДѓЃЌЫЕУїИФБфЕФЬѕМўЪЧдіДѓСЫN2O4ЕФХЈЖШЁЃ
(3)ИљОн(2)ПЩжЊЃЌ90 sКѓЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЛдіДѓN2O4ЕФХЈЖШЃЌдкКуШнШнЦїжаЯрЕБгкдіДѓбЙЧПЃЌдђN2O4ЕФзЊЛЏТЪМѕаЁЁЃ
(4)ДгЭМЯёПЩжЊЃЌNO2ЮЊЗДгІЮя,N2O4ЮЊЩњГЩЮяЁЃ60 sДяЕНЦНКтЪБNO2ЕФХЈЖШдіДѓСЫ0.120 molЁЄL-1ЃЌЫЕУїN2O4ЗДгІЙ§ГЬжаХЈЖШМѕЩйСЫ0.060 molЁЄL-1ЃЌвђЮЊвбжЊдк70 sЪБN2O4ЕФХЈЖШЮЊ0.040 molЁЄL-1ЃЌЫљвдN2O4ЕФЦ№ЪМХЈЖШЮЊ0.040 molЁЄL-1+
0.060 molЁЄL-1=0.100 molЁЄL-1ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ3-4Н№ЪєВФСЯгУЭО Н№ЪєПѓЮяРћгУСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЗжЮіЭЦРэЪЧЛЏбЇбЇЯАЕФЗНЗЈжЎвЛЁЃЯТСаЪЕбщЭЦРэжаЃЌе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎН№ЪєЕФвБСЖЗНЗЈгыН№ЪєЕФЛюЦУадгаКмДѓЙиЯЕЃЌЫљвдЬњЁЂаПЕШН№ЪєвЛАугУШШЛЙдЗЈвБСЖ
BЃЎФЦБШЭЛюЦУЃЌЫљвдФЦПЩвдДгСђЫсЭШмвКжажУЛЛГіЭ
CЃЎЙЄвЕЩЯЕчНтШлШкТШЛЏУОПЩжЦЕУН№ЪєУОЃЌЫљвдЙЄвЕЩЯЕчНтШлШкТШЛЏТСПЩжЦЕУТС
DЃЎНЋУОЬѕКЭТСЦЌгУЕМЯпСЌНгКѓВхНјЯЁNaOHШмвКжаЃЌУОЬѕЩЯВњЩњЦјХнЃЌЫЕУїТСБШУОЛюЦУ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 8-3бЮРрЕФЫЎНтСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
дкеєЗЂУѓжагУОЦОЋЕЦМгШШеєИЩЯТСаЮяжЪЕФШмвКШЛКѓзЦЩеЃЌПЩвдЕУЕНИУЮяжЪЙЬЬхЕФЪЧ( )
A.AlCl3 B.Na2SO3 C.KMnO4 D.MgSO4
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 8-1ШѕЕчНтжЪЕФЕчРыСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКЬюПеЬт
вбжЊ25 ЁцЪБВПЗжШѕЕчНтжЪЕФЕчРыЦНКтГЃЪ§Ъ§ОнШчБэЫљЪОЃК

ЛиД№ЯТСаЮЪЬтЃК
(1)ЮяжЪЕФСПХЈЖШОљЮЊ0.1 molЁЄL-1ЕФЫФжжШмвКЃК
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pHгЩаЁЕНДѓХХСаЫГађЪЧ (гУБрКХЬюаД)ЁЃ
(2)ГЃЮТЯТЃЌ0.1 mol/LЕФCH3COOHШмвКМгЫЎЯЁЪЭЙ§ГЬжаЃЌЯТСаБэДяЪНЕФЪ§ОнБфДѓЕФЪЧ ЁЃ
A.c(H+)
B.c(H+)/c(CH3COOH)
C.c(H+)ЁЄc(OH-)
D.c(OH-)/c(H+)
E.c(H+)ЁЄc(CH3COO-)/c(CH3COOH)
(3)ЬхЛ§ОљЮЊ100 mL pHЃН2ЕФCH3COOHгывЛдЊЫсHXЃЌМгЫЎЯЁЪЭЙ§ГЬжаpHгыШмвКЬхЛ§ЕФЙиЯЕШчЭМЫљЪОЃЌдђHXЕФЕчРыЦНКтГЃЪ§ (ЬюЁАДѓгкЁБЁЂЁАаЁгкЁБЛђЁАЕШгкЁБ)CH3COOHЕФЕчРыЦНКтГЃЪ§ЃЌРэгЩЪЧ ЁЃ

ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 8-1ШѕЕчНтжЪЕФЕчРыСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
НЋХЈЖШЮЊ0.1 molЁЄL-1 HFШмвКМгЫЎВЛЖЯЯЁЪЭЃЌЯТСаИїСПЪМжеБЃГждіДѓЕФЪЧ( )
A.c(H+) B.Ka(HF) C. D.
D.
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 7-2ЛЏбЇЦНКтзДЬЌЛЏбЇЦНКтвЦЖЏСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
дкФГКуШнЕФУмБеШнЦїжаЃЌПЩФцЗДгІA(g)ЃЋB(g) xC(g)гаШчЭМЫљЪОЕФЙиЯЕЧњЯпЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
xC(g)гаШчЭМЫљЪОЕФЙиЯЕЧњЯпЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ( )

A.ЮТЖШЃКT1ЃОT2 B.бЙЧПЃКp1ЃОp2
C.е§ЗДгІЪЧЮќШШЗДгІ D.xЕФжЕЪЧ2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 7-2ЛЏбЇЦНКтзДЬЌЛЏбЇЦНКтвЦЖЏСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
вбжЊЃК2SO2(g)+O2(g) 2SO3(g)ІЄH=-197 kJЁЄmol-1ЁЃЪЕбщВтЕУ4 mol SO2ВЮМгЩЯЪіЗДгІЗХГі354 kJШШСПЃЌдђSO2ЕФзЊЛЏТЪзюНгНќгк( )
2SO3(g)ІЄH=-197 kJЁЄmol-1ЁЃЪЕбщВтЕУ4 mol SO2ВЮМгЩЯЪіЗДгІЗХГі354 kJШШСПЃЌдђSO2ЕФзЊЛЏТЪзюНгНќгк( )
A.90% B.80% C.50% D.40%
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 6ЛЏбЇЗДгІгыФмСПСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
дк100 gЬПВЛЭъШЋШМЩеЫљЕУЦјЬхжаCOКЭCO2ЕФЬхЛ§БШЮЊ1ЁУ2ЁЃвбжЊЃК
CЃЈsЃЉЃЋ1/2O2ЃЈgЃЉ=COЃЈgЃЉ ІЄH1ЃНЃ110ЃЎ35 kJ/mol
COЃЈgЃЉЃЋ1/2O2 =CO2ЃЈgЃЉ ІЄH2ЃНЃ282ЃЎ57 kJ/mol
дђгы100 gЬПЭъШЋШМЩеЯрБШЃЌЫ№ЪЇЕФШШСПЪЧЃЈ ЃЉ
AЃЎ392ЃЎ93 Kj BЃЎ2 489ЃЎ42 kJ
CЃЎ784ЃЎ92 kJ DЃЎ3 274ЃЎ3 kJ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ФъЛЏбЇИпПМзмИДЯАПЮЪБбнСЗ 5-1дзгНсЙЙдзгКЫЭтЕчзгХХВМСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ДгКъЙлЗНУцПДЮяжЪЪЧгЩдЊЫизщГЩЕФЃЌДгЮЂЙлЗНУцПДЮяжЪЪЧгЩСЃзгЙЙГЩЕФЃЌЯТСагаЙиЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
A.дЊЫидзгЕФЖрбљадЪЧгЩЙЙГЩдзгЕФжЪзгКЭжазгЪ§ФПв§Ц№ЕФ
B.дЊЫиЕФЛЏбЇаджЪжївЊШЁОігкдЊЫидзгЕФзюЭтВуЕчзгЪ§
C.жЛгЩвЛжжЗжзгЙЙГЩЕФЮяжЪвЛЖЈЪЧДПОЛЮя
D.жЪзгЪ§ЕШгкЕчзгЪ§ЕФЮЂСЃЃЌПЩФмЪЧвЛжжЗжзгКЭвЛжжРызг
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com