
| A、6molA+2molB |
| B、1.5molA+0.5molB+1molC+0.5molD |
| C、3molA+1molB+2molC+1molD |
| D、1molB+2molC+1molD |


科目:高中化学 来源: 题型:
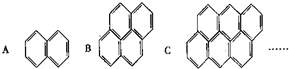 在沥青蒸气里含有多种稠环芳香烃,如图所示A、B、C …,
在沥青蒸气里含有多种稠环芳香烃,如图所示A、B、C …,查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、肯定不含有CO2 |
| B、只含有SO2和CO |
| C、含有SO2、CO和CO2,可能含HCl |
| D、含HCl、SO2和CO,可能含CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
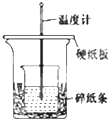 某实验小组学生用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如
某实验小组学生用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如| A、烧杯间填满碎纸条的作用是固定小烧杯 |
| B、图中装置还需要增加一根玻璃棒进行搅拌 |
| C、量取NaOH溶液的体积时仰视进行操作,会使测出的中和热数值偏高 |
| D、若改用60 mL 0.55 mol/L盐酸与40 mL 0.50 mol/L的NaOH溶液进行反应,从理论上讲测出的中和热不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某微粒空间构型为直线形,则该微粒一定是非极性分子 |
| B、某微粒空间构型为V形,则中心原子一定是sp3杂化 |
| C、某微粒空间构型为平面三角形,则中心原子一定是sp2杂化 |
| D、某微粒空间构型为正四面体,则键角一定是109°28’ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、与电子最近的金属阳离子 |
| B、整块金属的所有金属阳离子 |
| C、在电子附近的金属阳离子 |
| D、与电子有吸引力的金属阳离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com