
(14分)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用下图A装置制备乙酸乙酯.
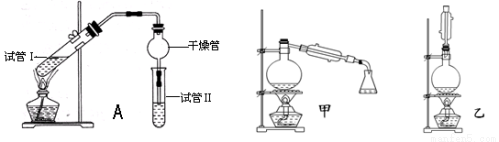
(1)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:
与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是 .
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层的厚度/cm |
A | 2mL乙醇、1mL乙酸、 | 饱和Na2CO3溶液 | 3.0 |
B | 2mL乙醇、1mL乙酸 | 0.1 | |
C | 2mL乙醇、1mL乙酸、 | 0.6 | |
D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.实验D中应加入盐酸的体积和浓度分别是 mL和 mol?L-1.
②分析实验 (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.
(3)若现有乙酸90g,乙醇138g发生酯化反应得到88g乙酸乙酯,试计算该反应的产率为 .
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图.图中( )内为适当的试剂,【 】内为适当的分离方法.
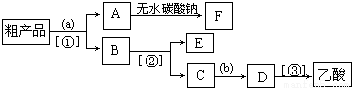
①试剂a是 ;分离方法②是 ,分离方法③是 .分离方法①是分液,在具体操作中应充分振荡,然后静置,待分层后 (填标号),
A.直接将乙酸乙酯从分液漏斗上口倒出
B.直接将乙酸乙酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸乙酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸乙酯从上口放出
②在得到的A中加入无水碳酸钠粉末,振荡,目的是 .
(5)为充分利用反应物,甲、乙两位同学分别设计了上面图中甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物).你认为最合理的是
(1)CH3COOH+CH3CH218OH CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O
冷凝和防止倒吸;(2)① 3; 4 ;② AC ;
(3) 66.7% ;(4) ①饱和Na2CO3溶液;蒸馏; 蒸馏; D; ②除去乙酸乙酯中混有的少量水(或干燥);(5)乙。
【解析】
试题分析:(1)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:CH3COOH+ CH3CH218OH  CH3CO18OC2H5+H2O;与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是冷凝和防止倒吸;(2)①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.由于在实验C中使用的硫酸是3mL 2mol?L-1,为了使条件与C相同,所以在实验D中应加入一元强酸盐酸的体积和浓度分别是3mL和4mol?L-1。②分析实验A、C 可知:其它条件相同只有硫酸的浓度不同,结构使用浓硫酸反应产生的酯多,说明浓H2SO4的吸水性提高了乙酸乙酯的产率;(3)n(乙酸)=90g÷60g/mol=1.5mol,n(乙醇)=138g÷46g/mol=3mol,由于乙醇过量,所以应该按照乙酸来计算得到的酯的质量。n(乙酸乙酯)=88g÷88g/mol=1mol,则该反应的产率为_1mol÷1.5mol)×100%=66.7%。(4)①试剂a是饱和Na2CO3溶液,通过分液分离得到:A是乙酸乙酯;B是含有乙醇、乙酸钠、碳酸钠的溶液;向乙酸乙酯中加入碳酸钠固体除去其中少量的水,然后过滤得到纯净的乙酸乙酯;将B蒸馏可以得到E:乙醇;溶液是乙酸钠、碳酸钠的溶液;向其中加入浓硫酸,得到乙酸、硫酸钠的混合物,利用二者沸点的不同,通过蒸馏就可以得到乙酸。分离方法①是分液,在具体操作中应充分振荡,然后静置,待分层后先将水层从分液漏斗的下口放出,再将乙酸乙酯从上口放出,故选项是D.②在得到的A中加入无水碳酸钠粉末,振荡,目的是除去乙酸乙酯中混有的少量水(或干燥);(5)为充分利用反应物,甲、乙两位同学分别设计了上面图中甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物).由于甲中未发生反应的乙酸乙醇都随着产生的酯挥发出去,所以物质的利用率降低,而乙都回流到反应装置,从而利用率大大提高,所以我认为最合理的是乙。
CH3CO18OC2H5+H2O;与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是冷凝和防止倒吸;(2)①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.由于在实验C中使用的硫酸是3mL 2mol?L-1,为了使条件与C相同,所以在实验D中应加入一元强酸盐酸的体积和浓度分别是3mL和4mol?L-1。②分析实验A、C 可知:其它条件相同只有硫酸的浓度不同,结构使用浓硫酸反应产生的酯多,说明浓H2SO4的吸水性提高了乙酸乙酯的产率;(3)n(乙酸)=90g÷60g/mol=1.5mol,n(乙醇)=138g÷46g/mol=3mol,由于乙醇过量,所以应该按照乙酸来计算得到的酯的质量。n(乙酸乙酯)=88g÷88g/mol=1mol,则该反应的产率为_1mol÷1.5mol)×100%=66.7%。(4)①试剂a是饱和Na2CO3溶液,通过分液分离得到:A是乙酸乙酯;B是含有乙醇、乙酸钠、碳酸钠的溶液;向乙酸乙酯中加入碳酸钠固体除去其中少量的水,然后过滤得到纯净的乙酸乙酯;将B蒸馏可以得到E:乙醇;溶液是乙酸钠、碳酸钠的溶液;向其中加入浓硫酸,得到乙酸、硫酸钠的混合物,利用二者沸点的不同,通过蒸馏就可以得到乙酸。分离方法①是分液,在具体操作中应充分振荡,然后静置,待分层后先将水层从分液漏斗的下口放出,再将乙酸乙酯从上口放出,故选项是D.②在得到的A中加入无水碳酸钠粉末,振荡,目的是除去乙酸乙酯中混有的少量水(或干燥);(5)为充分利用反应物,甲、乙两位同学分别设计了上面图中甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物).由于甲中未发生反应的乙酸乙醇都随着产生的酯挥发出去,所以物质的利用率降低,而乙都回流到反应装置,从而利用率大大提高,所以我认为最合理的是乙。
考点:考查实验室制取乙酸乙酯的反应原理、实验操作、混合物的分离、原料的利用率等知识。


科目:高中化学 来源:2013-2014河南省周口市高二下学期6月联考化学试卷(解析版) 题型:选择题
下列说法正确的是;
A.用石墨作电极,电解1mol/LNa2CO3的溶液,溶液的pH值保持不变
B.非金属元素呈现的最高化合价不超过该元素的最外层电子数
C.含8gNaOH的溶液中通入一定量的H2S后,将所得溶液小心蒸干,得无水物7.9g,则该无水物中一定含有Na2S
D.使用清洁的天然气是快速、有效地减缓大气中二氧化碳大量增加的生态学措施
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期5月联考化学试卷(解析版) 题型:选择题
W、X、Y、Z是短周期元素,其部分性质如下表

下列说法正确的是
A.气态氢化物的热稳定性:X>W B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W D.Z的氧化物中含有非极性共价键
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省南阳市春期高二期终质量评估化学试卷(解析版) 题型:选择题
氨甲环酸和氨甲苯酸是临床上常用的止血药,其结构如下图:
 、
、
下列说法错误的是
A.氨甲环酸、氨甲苯酸都既能溶于盐酸,又能溶于NaOH溶液
B.氨甲环酸、氨甲苯酸都能发生取代、氧化、缩聚等反应
C.氨甲环酸、氨甲苯酸中各有5种不同的氢原子
D.氨甲苯酸和苯丙氨酸互为同系物
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省南阳市春期高二期终质量评估化学试卷(解析版) 题型:选择题
下列物质中,既能与盐酸反应,又能与KOH溶液反应的是
①NaHCO3 ②AgNO3 ③(NH4)2S
④HOOC-COONa ⑤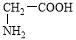 ⑥
⑥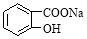
A.全部 B.①②④⑤⑥ C.②③④⑤⑥ D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省南阳市春期高一期终质量评估化学试卷(解析版) 题型:选择题
现有一包铝热剂是铝粉和氧化铁(Fe2O3)粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(假定反应前后溶液的体积不变):
①向其中一份固体中加入100 mL 2.0mol?L-1的NaOH溶液,加热使其充分反应后过滤,测得溶液中的c(OH-)=1mol?L-1
②向另一份固体中加入100 mL 4.0 mol?L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且c(H+)=0.1mol?L-1则产生的气体的体积(标准状况)为 ( )
A.2.856L B.2.448L C.2.688L D.2.352L
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省南阳市春期高一期终质量评估化学试卷(解析版) 题型:选择题
实验室制备,收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器口顺序为a接( )接( )接( )接( )接f(填接口字母) ( )

A.b c d e B.d e b c C.d e c b D.e d b c
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省六市毕业班第二次联合调研检测理综化学试卷(解析版) 题型:选择题
英国赫瑞瓦特大学陶善文博士研究出以尿素为动力的燃 料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,关于该电池描述正确的是

A.电池工作时H+移向负极
B.该装置还可以将电能转化成为化学能
C.理论上电池工作时,每消耗67.2L O2时,可以净化2mol CO(NH2)2
D.电池的负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省高二下学期第三次月考化学试卷(解析版) 题型:选择题
进行化学实验必须注意安全,下列说法不正确的是( )
A.点燃氢气前要检验纯度,以免发生爆炸
B.不慎将浓盐酸溅到皮肤上,要立即用浓碱溶液冲洗
C.CO气体有毒,处理CO尾气的方法一般是将其点燃,转化成无毒的CO2
D.在盛O2的集气瓶中进行铁丝燃烧实验时,事先在集气瓶底部铺上一层沙子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com