
| A. | 氢键是一种特殊化学键,它广泛地存在于自然界中 | |
| B. | 在 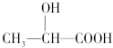 分子中含有1个手性C原子 分子中含有1个手性C原子 | |
| C. | 碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子 | |
| D. | 含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大 |
分析 A.氢键为分之间作用力的一种;
B.1个C上连4个不同的原子或者原子团为手性碳原子;
C.依据相似相溶原理解答;
D.含氧酸可用通式XOm(OH)n来表示,式中m大于等于2的是强酸,m为0的是弱酸,据此可知,非羟基氧原子数目越大,酸性越强.
解答 解:A.氢键为分之间作用力的一种,氢键不是化学键,故A错误;
B. 分子中中间碳原子,上连4个不同的原子或者原子团,为手性碳原子,含有1个手性C原子,故B正确;
分子中中间碳原子,上连4个不同的原子或者原子团,为手性碳原子,含有1个手性C原子,故B正确;
C.碘是非极性分子,水是极性分子,二者极性不同,所以碘不易溶于水,故C错误;
D.含氧酸可用通式XOm(OH)n来表示,式中m大于等于2的是强酸,m为0的是弱酸,据此可知,非羟基氧原子数目越大,酸性越强,故D错误;
故选:B.
点评 本题考查分子间作用力和分子的极性、手性C原子,根据非羟基氧原子数目多少来确定酸性强弱即可,难度不大.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:推断题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
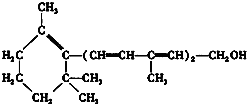
| A. | 维生素A是一种酚 | |
| B. | 维生素A的一个分子中有三个双键 | |
| C. | 维生素A可以使酸性高锰酸钾溶液褪色 | |
| D. | 维生素A具有环己烷的结构单元 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
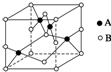 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com