
向FeBr2、FeI2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示,下列有关说法中不正确的是( )
A.d曲线代表溶液中Br-变化情况
B.原溶液中FeI2的物质的量为2 mol
C.原溶液中n(Fe2+):n(Br-)=2:3
D.当通入2 mol Cl2时,溶液中离子反应为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
解析 由于Fe2+、I-、Br-的还原性大小为:I->Fe2+>Br-,故向该溶液中通入氯气,氯气先氧化I-,再氧化Fe2+,最后氧化Br-。故a、b、c、d曲线分别表示I-、Fe2+、Fe3+、Br-的变化情况,A项正确;由图象可知,I-为2 mol,故原溶液中FeI2为1 mol,B项错误;由图可以看出Fe2+是4 mol,Br-是6 mol,故原溶液中n(Fe2+):n(Br-)=2:3,C项正确;当通入2 mol Cl2时,2 mol的I-消耗氯气1 mol,余下的1 mol氯气再与2 mol Fe2+反应,故溶液中发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-,D项正确。
答案 B


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:
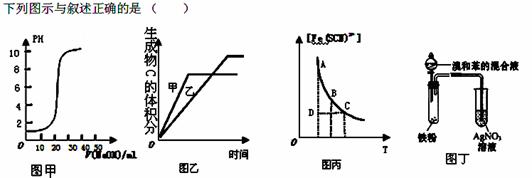
A.图甲表示用0.1000mol/L的NaOH溶液滴定20.00ml,0.1000mol/L的醋酸溶液得到的滴定曲线
B.图乙表示压强对可逆反应2A (g)+ B (g) 3C (g)+D (s)的影响且甲的比乙的压强大
3C (g)+D (s)的影响且甲的比乙的压强大
C.图丙表示可逆反应Fe3+(aq)+SCN—(aq) Fe(SCN)2+(aq)平衡时,物质的量浓度
Fe(SCN)2+(aq)平衡时,物质的量浓度
[Fe(SCN) 2+]与温度T的关系,反应处于D点时,一定有V(正)>V(逆)
D.图丁所示装置可证明溴与苯发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
分类是化学学习与研究的常用方法,下列分类正确的是( )
A.非金属氧化物均属于酸性氧化物
B.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
C.根据电解质的水溶液导电性的强弱,将电解质分为强电解质和弱电解质
D.根据反应物和生成物的类别以及反应前后物质种类的多少,把化学反应分为化合反应、分解反应、置换反应和复分解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有Mn2+的酸性溶液中滴加过二硫酸钾(K2S2O8)溶液,会发生如下反应(未配平):Mn2++S2O +H2O―→MnO
+H2O―→MnO +SO
+SO +H+。下列说法正确的是( )
+H+。下列说法正确的是( )
A.该反应中起氧化作用的是Mn2+
B.反应中有1 mol还原剂参加反应时,转移的电子物质的量为4 mol
C.反应后溶液的pH降低
D.该反应常用于检验溶液中Mn2+的存在,现象是溶液紫红色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
高锰酸钾(KMnO4)和过氧化氢(H2O2)是两种典型的氧化剂。
(1)H2O2的结构式为________________。
(2)下列物质中能使酸性KMnO4溶液褪色的是________(填选项字母)。
A.臭碱(Na2S) B.小苏打(NaHCO3)
C.水玻璃(Na2SiO3) D.酒精(C2H5OH)
(3)高锰酸钾、双氧水、活性炭常用于饮用水的处理,但三者联合作用时必须有先后顺序。
①在稀硫酸中,KMnO4和H2O2能发生氧化还原反应:
氧化反应:H2O2-2e-―→2H++O2↑
还原反应:MnO +5e-+8H+―→Mn2++4H2O
+5e-+8H+―→Mn2++4H2O
写出该氧化还原反应的离子方程式_____________________________
____________________________________________________________。
②在处理饮用水时,活性炭应在高锰酸钾反应结束后投加,否则会发生反应:KMnO4+C+H2O―→MnO2+X+K2CO3(未配平),其中X的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,正确的是( )
A.向NaOH溶液中加入少量Mg(HCO3)2溶液:2OH-+Mg2+===M g(OH)2↓
g(OH)2↓
B.向足量NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液:HCO +Ba2++H++SO
+Ba2++H++SO ===BaSO4↓+H2O+CO2↑
===BaSO4↓+H2O+CO2↑
C.酸性KMnO4溶液与H2O2反应:2MnO +10H++3H
+10H++3H 2O2===2Mn2++3O2↑+8H2O
2O2===2Mn2++3O2↑+8H2O
D.向Fe(NO3)3溶液中加入过量HI溶液:Fe3++3NO +12H++10I-===Fe2++3NO↑+5I2+6H2O
+12H++10I-===Fe2++3NO↑+5I2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
铜是重要的工业原材料,现有Cu、Cu2O组成的混合物,某研究性学习小组为了探究其组成情况,取35.2 g混合物加入0.5 L 3.4 mol/L的稀硝酸,固体物质完全反应,生成4.48 L(标准状况)的NO。向所得溶液中加入a L 2.0 mol/L的NaOH溶液,恰好使溶液中的Cu2+沉淀完全。
(1)Cu2O与稀硝酸反应的化学方程式为________________。
(2)混合物中,n(Cu)=________;n(Cu2O)=________。
(3)所加NaOH溶液的体积a L=________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池反应原理为:Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l),下列说法正确的是( )
2PbSO4(s)+2H2O(l),下列说法正确的是( )
A.放电时,负极的电极反应式为:Pb-2e-===Pb2+
B.放电时 ,正极得电子的物质是PbO2
,正极得电子的物质是PbO2
C.充电时,电解质溶液中硫酸浓度减小
D.充电时,阴极的电极反应式为PbSO4-2e-+2H2O===PbO2+4H++SO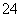
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com