
【题目】常温下联氨![]() 的水溶液中有:
的水溶液中有:
![]()
![]()
![]()
![]() 提示:二元弱碱的电离也是分步电离
提示:二元弱碱的电离也是分步电离![]()
该溶液中的微粒的物质的量分数![]() 随
随![]() 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是![]()
![]()
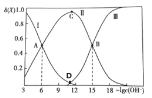
A.据A点可求:![]()
B.D点溶液的 ![]()
C.若C点为![]() 溶液,则存在:
溶液,则存在:![]()
D.在![]() 水溶液中,
水溶液中,![]()
【答案】B
【解析】
已知联氨的两步电离分别为:N2H4+H2O![]() N2H5++OH-,N2H5++H2O
N2H5++OH-,N2H5++H2O![]() N2H62++OH-.曲线Ⅰ为N2H4、Ⅱ为N2H5+、Ⅲ为N2H62+;
N2H62++OH-.曲线Ⅰ为N2H4、Ⅱ为N2H5+、Ⅲ为N2H62+;
A.K1= 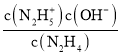 ,A点N2H5+和N2H4的物质的量分数相等,则c(N2H5+)=c(N2H4),K1=c(OH-)=10-6,故A正确;
,A点N2H5+和N2H4的物质的量分数相等,则c(N2H5+)=c(N2H4),K1=c(OH-)=10-6,故A正确;
B.K2=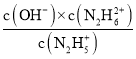 ,B点c(N2H5+)=c(N2H62+),则K2=c(OH-)=10-15;①N2H4+H2O
,B点c(N2H5+)=c(N2H62+),则K2=c(OH-)=10-15;①N2H4+H2O![]() N2H5++OH-,②N2H5++H2O
N2H5++OH-,②N2H5++H2O![]() N2H62++OH-,①+②得N2H4+2H2O
N2H62++OH-,①+②得N2H4+2H2O![]() N2H62++2OH-,则K1×K2=
N2H62++2OH-,则K1×K2= = 10-6×10-15=10-21,在D点c(N2H4)= c(N2H62+),故c(OH-)=
= 10-6×10-15=10-21,在D点c(N2H4)= c(N2H62+),故c(OH-)=![]() =10-10.5,故B错误;
=10-10.5,故B错误;
C.N2H5Cl溶液中存在电荷守恒:c(OH-)+c(Cl-)=c(H+)+c(N2H5+)+2c(N2H62+),C点显酸性,c(H+)>c(OH-),c(Cl-)>(N2H5+)+2c(N2 H62+),故C正确;
D.在N2N5Cl的水溶液中,存在电荷守恒c(OH-)+c(Cl-)=c(H+)+c(N2H5+)+2c(N2H62+)和物料守恒:c(Cl-)=c(N2H4)+c(N2H5+)+c(N2H62+),则c(OH-)+ c(N2H4)+c(N2H5+)+c(N2H62+)=c(H+)+c(N2H5+)+2c(N2H62+)得c(OH-)+ c(N2H4)=c(H+)+ c(N2H62+),故D正确;
故答案为B。


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】已知:Ⅰ![]() 的燃烧热为
的燃烧热为![]()
Ⅱ![]()
![]()
![]()
Ⅲ![]()
![]()
则![]() ______。
______。
![]() 对于可逆反应
对于可逆反应![]() 采取以下措施可以提高
采取以下措施可以提高![]() 产率的是______
产率的是______![]() 填字母
填字母![]()
A.降低体系的温度![]() 压缩容器的体积
压缩容器的体积![]() 减少水量
减少水量![]() 选用适当的催化剂
选用适当的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,下列说法正确的是![]()
![]()
A.在滴有酚酞溶液的氨水里,加入![]() 至溶液恰好无色,则此时溶液的
至溶液恰好无色,则此时溶液的![]()
B.同![]() 的溶液:
的溶液:![]() 溶液,物质的量浓度最大的是
溶液,物质的量浓度最大的是![]()
C.有两种酸HA和HB,已知HA的酸性比HB弱,在物质的量浓度均为![]() 的NaA和NaB混合溶液中,有
的NaA和NaB混合溶液中,有![]()
D.pH相同的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液、NaOH溶液,其浓度大小关系为:
溶液、NaOH溶液,其浓度大小关系为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,其产量可以用来衡量一个国家的石油化工发展水平。A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据如图回答下列问题:
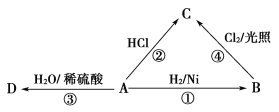
(1)写出A的电子式及空间构型:电子式___,空间构型___。
(2)②、④两种制备氯乙烷的方法中,方法___好。原因是__。
(3)写出③、④两步反应的化学方程式,并注明反应类型:
③___,反应类型___。
④__,反应类型__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,向 ![]() 二元弱酸
二元弱酸 ![]() 溶液中滴加
溶液中滴加 ![]() 溶液,溶液中的
溶液,溶液中的 ![]() ,
,![]() ,
, ![]() 的物质的量分数
的物质的量分数![]()
![]() 随 pH的变化如图所示。下列说法错误的是
随 pH的变化如图所示。下列说法错误的是![]()
![]()

![]() 已知
已知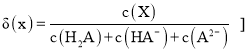
A.加入 ![]() 时,
时,![]()
B.当 ![]() ,
, ![]()
C.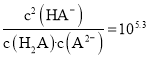
D.当混合溶液呈中性时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向一定浓度的Na2X溶液中滴入盐酸,溶液的pH与离子浓度变化关系如图所示。
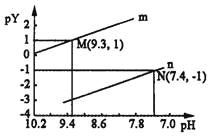
已知:H2X是二元弱酸,Y表示![]() 或
或![]() ,pY=﹣lgY.下列叙述不正确的是( )
,pY=﹣lgY.下列叙述不正确的是( )
A. 曲线n表示pH与p![]() 的变化关系
的变化关系
B. Ka2(H2X)=1.0×10﹣10.3
C. NaHX溶液中c(H+)>c(OH﹣)
D. 当溶液呈中性时,c(Na+)=c(HX﹣)+2c(X2﹣)+c(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。下列说法不正确的是

A. 3种HCl溶液的c(HCl):最大的是最小的100倍
B. 曲线a、b、c对应的c(NaOH):a>b>c
C. 当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)
D. 当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+3B(g)![]() 2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A.v(A)=0.02 mol/(L·s) B.v(B)=0.03 mol/(L·s)
C.v(B)=0.90 mol/(L·min) D.v(C)=0.60 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组学生用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算中和热。下列说法正确的是( )

A.如图条件下实验过程中没有热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的作用是固定小烧杯
D.若改用60mL0.50mol/L盐酸与50mL0.55mol/L的NaOH溶液进行反应,从理论上说所测反应热数值是相等的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com