
| A. | 溶液中含有2mol K2SO4 | B. | 可将2mol K2SO4溶于1L水中制得 | ||
| C. | 溶液中c(K+ )=4 mol•L-1 | D. | 1L 溶液中含4molK+,4molSO42- |
分析 2mol•L-1 K2SO4溶液表示1L溶液中含有2molK2SO4,K2SO4可电离出钠离子和硫酸根离子,结合物质的构成计算.
解答 解:A.体积不确定,不能确定物质的量,故A错误;
B.可将2mol K2SO4溶于1L水中制得,溶液体积大于1L,浓度小于2mol/L,故B错误;
C.溶液中c(K+ )=2c(K2SO4)=4 mol•L-1,故C正确;
D.1L 溶液中含4molK+,2molSO42-,故D错误.
故选C.
点评 本题考查学生对物质的量浓度的理解,为高频考点,侧重于学生的分析能力的考查,难度较小,注意物质的量浓度定义中体积是溶液体积不是溶剂体积,物质溶于水溶质可能会变化.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 工业合成氨时采用铁触媒作反应的催化剂 | |
| C. | 工业生产硫酸的过程中使用过量的空气以提高SO2的转化率 | |
| D. | 将收集NO2气体的烧瓶密闭后放在装有热水的烧杯中,发生颜色变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | Na2O2与 H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| C. | 氯气与水反应:Cl2+H2O═Cl-+2H++ClO- | |
| D. | 碳酸镁与稀盐酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取NaCl固体2.9 g | |
| B. | 胶头滴管加水定容时,有少量水滴到容量瓶外 | |
| C. | 定容时俯视读数 | |
| D. | 称量固体时,天平的两个托盘上放两张质量相等的纸片,其他操作均正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢原子的结构示意图为: ;则反氢原子的结构示意图为: ;则反氢原子的结构示意图为: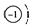 | |
| B. | 反氢原子中有一个带负电荷的反质子和一个带正电荷的反电子 | |
| C. | 反氢原子的摩尔质量为1g/mol | |
| D. | 21H的反氢原子中有2个带负电荷的反质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶中有少量蒸馏水 | |
| B. | 溶液从烧杯转移到容量瓶后没有洗涤烧杯 | |
| C. | 未冷却即将溶液转移到容量瓶 | |
| D. | 定容时俯视容量瓶刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
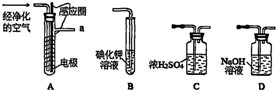
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com