
| A. | FeO和HNO3 | B. | Al(OH)3与HNO3 | C. | H2S和HNO3 | D. | NH3与HNO3 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
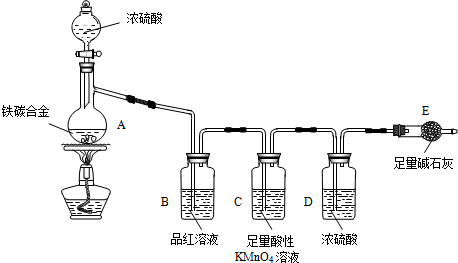
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢极易溶于水 | B. | 液态氯化氢不能导电 | ||
| C. | 氯化氢在水溶液中完全电离 | D. | 氯化氢是无色有刺激性气味的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素位于周期表第5周期第IB族 | B. | 该元素原子核外有5个电子层 | ||
| C. | 该元素原子最外层共有3个电子 | D. | 该元素原子M层上共有8个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH3Cl、CH2Cl2.CHCl3.CCl4互为同系物 | |
| B. | O2和O3互为同素异形体 | |
| C. | 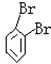 和 和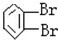 互为同分异构体 互为同分异构体 | |
| D. | 1H、2H、3H互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C=$\frac{1000wρ}{M}$ | B. | w%=$\frac{CM}{1000ρ}$% | C. | C=$\frac{m}{VM}$ | D. | m=$\frac{V•ρw}{100}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| B | ||
| A | C |
| A. | A为ⅣA族元素 | |
| B. | B是同主族中化学性质最活泼的非金属 | |
| C. | B为第二周期的元素 | |
| D. | 三种元素都为非金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com