
����Ŀ��ijʵ����Ҫ500mL0.10mol/L��Na2CO3��Һ����ͨ�����²������ƣ�
�ٰѳ����õĹ���Na2CO3����С�ձ��У�����������ˮ�����ܽ⣻
������������ˮϴ���ձ��Ͳ�����2~3�Σ�ÿ��ϴ�ӵ�Һ�嶼С��ת������ƿ��������ҡ�ȣ�
�۸Ǻ�ƿ�����������µߵ���ҡ�ȣ�
�ܰ��ܽ�����������Һ��ȴ�����£�ת������A�У�
�ݼ���������ˮ��Һ���̶���1~2cm�������ý�ͷ�ιܵμ�����ˮ����Һ�İ�Һ����̶������У�
��1�������������ȷ˳��Ϊ__(�����)��
��2��������Na2CO3��������ӦΪ__g��
��3������A��������__��
��4��ȡ��100mL���ƺõ���Һ��������ˮϡ����c(Na2CO3)=0.02mol/L����ϡ�ͺ���Һ�����Ϊ__��
��5�����й�������ƿ��ʹ�÷����У���ȷ����__(����ĸ���)��
A.ʹ��ǰҪ�����Ƿ�©ˮ
B.������ƿ��ֱ���ܽ�����ϡ��Һ��
C.���ձ����ܽ�����Ѹ�ٽ���Һת�Ƶ�����ƿ��
D.������ƿ��ת����Һ�ò���������
E.��ˮʱˮ�������˿̶��ߣ�Ѹ���ý�ͷ�ιܽ�������ˮ����
��6�����в�����ʹ������Һ�����ʵ���Ũ��ƫ�͵���__(����ĸ���)��
A.���ձ��е���Һת�Ƶ�����ƿʱ������������ƿ��
B.���ݶ���ʱ����������ƿ�ϵĿ̶���
C.��ˮ����ʱ��ˮ�������˿̶���
D.ϴ�Ӳ����У�ϴ��Һû��ת������ƿ
���𰸡��٢ܢڢݢ� 5.3g 500mL����ƿ 500mL AD ACD
��������
��1������һ�����ʵ���Ũ����Һ�IJ���Ϊ���㡢�������ܽ⡢��ȴת�ơ�ϴ�ӡ����ݡ�ҡ�ȣ����Բ����������ȷ˳��Ϊ���٢ܢڢݢۣ��ʴ�Ϊ���٢ܢڢݢۡ�
��2������500mL0.10mol/L��Na2CO3��Һ�����ʵ���Ϊ0.05mol��������Ϊ5.3g�����Գ�����Na2CO3��������ӦΪ5.3g���ʴ�Ϊ��
5.3��
��3�������Ϊ��ȴת�ƵĹ��̣���Һ��ȴ�����º�С��ת��500mL������ƿ�У���������A��������500mL����ƿ���ʴ�Ϊ��
500mL����ƿ��
��4����Һϡ��ǰ�����ʵ����ʵ������䣬����ϡ�ͺ���Һ���Ϊ![]() ��
��
�ʴ�Ϊ��500mL��
��5��A. ʹ������ƿ֮ǰҪ����Ƿ�©ˮ��A��ȷ��
B. �ܽ�����ϡ��Һ��Ҫ���ձ��н��У�����������ƿ�У�B����
C. ���ձ����ܽ�����Ҫ����Һ�¶���ȴ�����º���ת��������ƿ�У�C����
D. ������ƿ��ת����ҺʱҪ�ò�����������D��ȷ��
E. ��ˮʱˮ�������˿̶��ߣ�Ӧ����������Һ��E���ʴ�Ϊ��AD��
��6��A. ���ձ��е���Һת�Ƶ�����ƿʱ������������ƿ�⣬���ʵ����ʵ������٣�������Һ�����ʵ���Ũ��ƫ�ͣ�A��ȷ��
B. ���ݶ���ʱ����������ƿ�ϵĿ̶��ߣ�������Һ�����ƫС�������ʵ���Ũ��ƫ�ߣ�B����
C. ��ˮ����ʱ��ˮ�������˿̶��ߣ�������Һ�����ƫ�������ʵ���Ũ��ƫ�ͣ�C����
D. ϴ�Ӳ����У�ϴ��Һû��ת������ƿ�����ʵ����ʵ������٣�������Һ�����ʵ���Ũ��ƫ�ͣ�D��ȷ���ʴ�Ϊ��ACD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������һ����MnO2����������Ũ�����ڼ��������³�ַ�Ӧ��ȡ2.24L��״���µ��������䷴Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O����(���ԭ������O-16��Mn-55)
MnCl2+Cl2��+2H2O����(���ԭ������O-16��Mn-55)
�Լ��㣺
(1)�μӷ�Ӧ��MnO2������____________��
(2)��Ӧ����Һ�����Ϊ100mL����Һ��MnCl2�����ʵ���Ũ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ҵ�����к���CO��CO2��N2��SO2�����壬��Na2SO3��Һ���ղ�����SO2�Ĺ�������ͼ��ʾ��
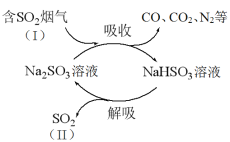
��1��SO2��Ũ�ȣ�I________II���������������
��2������������п���ѭ��ʹ�õ�������________��
��3���������չ�������Ҫ��Ӧ�Ļ�ѧ����ʽ��________��
��4������������Ҫ���ȣ�����������г���������SO42-������
�� ֤�������к�SO42-��ʵ�鷽���ǣ�ȡ���������������Һ��________�������������
�� ����SO42-��ԭ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С��������װ���Ʊ��屽������˵���������

A. װ��A�г��������ܽ��������������ã�װ��B�е�ʵ��������CCl4����ɫ���ɫ
B. ��װ��B������װ��C��װ��C�����ɵ���ɫ��������֤��װ��A�з���ȡ����Ӧ
C. ��װ��B������װ��D����װ��D������������β��
D. ��Ӧ���װ��A�м���NaOH��Һ�����ã��²�Ϊ��ɫ��״Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�������ӦA(g)��B(g)![]() C(g)����H<0���ﵽƽ����������ͼ���жϣ�
C(g)����H<0���ﵽƽ����������ͼ���жϣ�
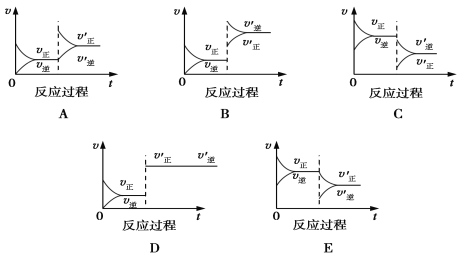
��1����ʾ�����¶ȣ��ﵽ��ƽ�����________(�A������B������C������D����E������ͬ)����ƽ����C����������________(���������С�����䡱����ͬ)��
��2����ʾ����ѹǿ���ﵽ��ƽ�����________��A��ת����________��
��3����ʾ����C�������ﵽ��ƽ�����______________��
��4����ʾ����A�������ﵽ��ƽ�����___________����ʱB��ת����__________��A��ת����___________��
��5����ʾʹ�ô������ﵽ��ƽ�����________________��C����������________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��![]() ��
��![]() ��
��![]() �����ڱ��е����λ����ͼ��ʾ����֪
�����ڱ��е����λ����ͼ��ʾ����֪![]() Ԫ��ԭ�ӵ���Χ�����Ų�ʽΪ
Ԫ��ԭ�ӵ���Χ�����Ų�ʽΪ![]() ��������˵������ȷ���ǣ� ��
��������˵������ȷ���ǣ� ��

A.![]() Ԫ��ԭ�ӵļ۵����Ų�ʽΪ
Ԫ��ԭ�ӵļ۵����Ų�ʽΪ![]()
B.![]() Ԫ����Ԫ�����ڱ��ĵ������ڵڢ�A��
Ԫ����Ԫ�����ڱ��ĵ������ڵڢ�A��
C.![]() Ԫ�����������������ǽ���Ԫ�����
Ԫ�����������������ǽ���Ԫ�����
D.![]() Ԫ��ԭ�ӵĺ�������Ų�ʽΪ
Ԫ��ԭ�ӵĺ�������Ų�ʽΪ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ������ȥ��Ӧ���ǣ���Ӧ����ʡ�ԣ��� ��
A.![]() -CH3CH2OH ��
-CH3CH2OH ��![]() -CH2=CH2��+ H2O
-CH2=CH2��+ H2O
B.CH3CH2CH3 + Br2��CH3CH2CH2Br + HBr
C.CH3CH2CHO + H2��CH3CH2CH2OH
D.2CH3CH2CH2OH + 2O2��CH3CH2CHO + 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ɶ�����Ⱦ���γɣ����а������������PM 2.5���ڣ����������NOx����CO��SO2�ȡ���ѧ�ڽ��������Ⱦ��������Ҫ�����á�
�� ��֪��2SO2(g) + O2(g) ![]() 2SO3(g) ��H =��196.6kJmol��1
2SO3(g) ��H =��196.6kJmol��1
2NO(g) + O2(g) ![]() 2NO2(g) ��H =��113.0kJmol��1
2NO2(g) ��H =��113.0kJmol��1
��ӦNO2(g) + SO2(g) ![]() SO3(g) + NO(g) ��H =__________kJmol��1��
SO3(g) + NO(g) ��H =__________kJmol��1��
һ�������£���NO2��SO2�������1:2���ں��º��ݵ��ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����__________��
a����ϵ�ܶȱ��ֲ��� b�����������ɫ���ֲ���
c��SO2��NO������ȱ��ֲ��� d��ÿ����1mol SO3��ͬʱ����1mol NO2
���������Ӧƽ��ʱNO2��SO2�����Ϊ1:5����ƽ�ⳣ��K=________________��
�� CO��CO2�������ںϳɼ״����״�������Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϣ������꿪���ļ״�ȼ�ϵ�ز��ò����缫����������е����ӽ���Ĥֻ�������Ӻ�ˮ����ͨ�����乤��ԭ����ʾ��ͼ��ͼ1��ʾ���ش��������⡣

�� Pt(a)�缫�ǵ�ص�______�����缫��ӦʽΪ��_________________��
�� ����õ�ع���ʱ��·��ͨ��2 mol���ӣ������ĵ�CH3OH��________mol��
�� CO���ںϳɼ״���Ӧ����ʽΪ��CO(g) + 2H2(g)![]() CH3OH (g) ��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ2��ʾ��ʵ�ʵ���������������250����1.3��104kPa���ң�ѡ���ѹǿ��������____________��
CH3OH (g) ��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ2��ʾ��ʵ�ʵ���������������250����1.3��104kPa���ң�ѡ���ѹǿ��������____________��
�� ͼ3��һ����NH3�ѳ�������NO��ԭ����
�� ������ԭ���У�NO����ת��ΪH2O��__________���ѧʽ����
�� ������2mol NH3��0.5mol O2ʱ����ȥ��NO�ڱ�״���µ����Ϊ__________L��
�� NOֱ�Ӵ��ֽ⣨����N2��O2��Ҳ��һ������;�����ڲ�ͬ�����£�NO�ķֽ���ﲻͬ���ڸ�ѹ�£�NO��40���·ֽ��������ֻ������ϵ�и�������ʵ�����ʱ��仯������ͼ4��ʾ��д��NO�ֽ�Ļ�ѧ����ʽ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д���������ʵ����ƣ�
A.(CH3)3CCH(CH3)(CH2)2CH(C2H5)2 A��������________��
B.(CH3)3CC��CCH2CH3 B��������____��
C.![]() C��������_____
C��������_____
D.CH2OHCH(C2H5) CH2OH D��������________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com