
【题目】按要求回答下列问题:
(1) CH2=CHCH=CH2的系统命名为______________;
(2)3—甲基—2一戊烯的结构简式为______________;
(3)![]() 的分子式为______________;
的分子式为______________;
(4)某烃的分子式为C4H4,它是合成橡胶的中间体,它有多种同分异构体
①试写出它的一种链式结构的同分异构体的结构简式______________.
②它有一种同分异构体,每个碳原子均达饱和,且碳与碳的夹角相同,该分子中碳原子形成的空间构型为______________形
【答案】1,3—丁二烯  C4H8O CH2=CH-C≡CH 正四面体
C4H8O CH2=CH-C≡CH 正四面体
【解析】
(1)烯烃命名时应选含有碳碳双键的最长碳链为主链,官能团碳碳双键的位次最小;
(2)根据烯烃的命名原则进行解答,注意编号从距离碳碳双键最近的一端开始;
(3)由结构简式书写分子式。
(4)①由链式结构可知含双键和三键;
②它的一种同分异构体,每个碳均达饱和,且构成的空间构型中碳与碳间的夹角都相同,则4个C形成正四面体结构。
(1)烯烃命名时应选含有碳碳双键的最长碳链为主链,官能团碳碳双键的位次最小,则CH2=CHCH=CH2的系统命名为1,3—丁二烯,故答案为:1,3—丁二烯;
(2)3—甲基—2一戊烯的主链上有5个碳原子,碳碳双键在2、3号碳原子上,3号碳连有一个甲基,则结构简式为 ,故答案为:
,故答案为: ;
;
(3)由结构简式可知,![]() 的分子式为C4H8O,故答案为:C4H8O;
的分子式为C4H8O,故答案为:C4H8O;
(4)①由链式结构,C4H4分子中可知含有碳碳双键和碳碳三键,结构简式为HC≡C-CH═CH2,故答案为:HC≡C-CH═CH2;
②它的一种同分异构体,每个碳均达饱和,且构成的空间构型中碳与碳间的夹角都相同,则4个C形成正四面体结构结构式为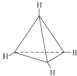 ,故答案为:正四面体。
,故答案为:正四面体。


科目:高中化学 来源: 题型:
【题目】综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如图所示:
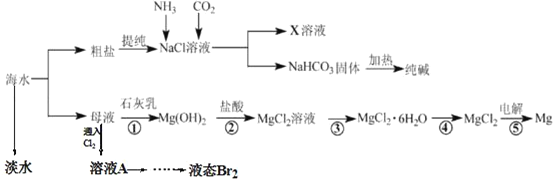
(1)从海水中获得淡水的装置如图,其中有_____处错误。

(2)在母液中通入氯气的离子方程式为_____,从溶液A中提取Br2,需要的主要仪器是____
(3)操作③是_____
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质。
①为制得纯净的NaCl晶体,操作如下:
a.溶解;
b.依次加入过量的_____溶液、NaOH溶液、_____溶液;
c._____;
d.加适量盐酸;
e._____(请补全缺少的试剂和实验步骤)
②步骤b中,加入最后一种试剂发生反应的离子方程式为_____
(5)用这种方法制得的Na2CO3中有少量的NaCl,检验NaCl的实验为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL0.1mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中逐滴滴入0.1mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是

A. a点时溶液中所含主要溶质为(NH4)2SO4
B. a→b段发生反应的离子方程式是 SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C. b点为最大沉淀量,对应的纵坐标值为0.02
D. c点加入Ba(OH)2溶液的体积为200 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。已知:SeO2在常温下是白色的晶体,熔点为340-350℃,则SeO2晶体属于____晶体,SeO2中Se原子采取的杂化类型为___。
(二)A、X、Y、Z、W、M、G等原子序数一次增大的前四周期元素
元素 | 相关信息 |
A | 原子核外电子总数与其周期数相同 |
X | 其羞态原子的L层中有3个未成对电子 |
Y | 荃态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反 |
Z | 原子核外p电子数比s电子数多l个 |
W | 原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817 I3=2745 I4=11575 |
M | 元素的主族数与周期数相差4 |
G | 其基态原子最外层电子数为1,其余各电子层均充满电子 |
(1)画出W基态原子的核外电子排布图______。
(2)A2Y的VSEPR模型名称为____。
(3)已知为X2Y分子中Y原子只与一个X原子相连,请根据等电子原理,写出X2Y的电子式____。
(4)X、G形成的某种化合物的晶胞结构如图所示,则其化学式为______。

(5)已知Z和M形成的化合物的晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的Z离子中心间距离为_____cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiH2PO4是制备电池的重要原料。室温下,LiH2PO4溶液的pH随c初始(H2PO4–)的变化如图1所示,H3PO4溶液中H2PO4–的分布分数δ随pH的变化如图2所示,[![]() ]下列有关LiH2PO4溶液的叙述正确的是
]下列有关LiH2PO4溶液的叙述正确的是


A. 溶液中存在3个平衡
B. 含P元素的粒子有H2PO4–、HPO42–、PO43–
C. 随c初始(H2PO4–)增大,溶液的pH明显变小
D. 用浓度大于1 mol·L-1的H3PO4溶液溶解Li2CO3,当pH达到4.66时,H3PO4几乎全部转化为LiH2PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活污水中的氮和磷主要以铵盐和磷酸盐的形式存在,可用电解法从溶液中除去。有Cl-存在时。除氮原理如图1所示。主要依靠有效氯(HClO、ClO-)将NH4+或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。
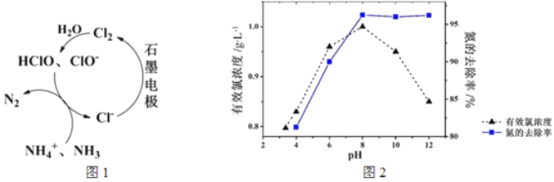
下列说法不正确的是
A. pH=3时,主要发生ClO-氧化NH3的反应
B. pH>8时,有效氯浓度随pH的增大而减小
C. pH>8时,NH4+转变为NH3·H2O,且有利于NH3逸出
D. pH<8时,氮的去除率随pH的减少而下降的原因是c(HClO)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3![]() 2HNO3+4N2↑+9H2O,下列说法正确的是( )
2HNO3+4N2↑+9H2O,下列说法正确的是( )
A. 分解反应都是氧化还原反应B. N2是还原产物,HNO3是氧化产物
C. 被氧化与被还原的氮原子数之比为3∶5D. 每生成4mol N2转移15mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质或物质间反应可能包括多步反应,其总的离子方程式正确的是
A. 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O===HClO+HSO3-
B. Na2S投入水中:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C. 向含1 mol AlCl3溶液中投入4 mol Na:Al3++4Na+2H2O===AlO2-+4Na++2H2↑
D. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-===Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家开发出一种低成本光伏材料—蜂窝状石墨烯。生产原理是Na2O+2CO  Na2CO3+C(石墨烯),然后除去Na2CO3,即可制得蜂窝状石墨烯。下列说法不正确的是( )
Na2CO3+C(石墨烯),然后除去Na2CO3,即可制得蜂窝状石墨烯。下列说法不正确的是( )
A.该生产石墨烯的反应属于氧化还原反应
B.石墨烯与金刚石互为同素异形体
C.Na2O属于碱性氧化物,CO属于酸性氧化物,Na2CO3属于盐
D.自然界中钠元素以化合态形式存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com