
分析 该原电池中,锌电极上电极反应式为Zn-2e-=Zn2+,铜电极上电极反应式为2H++2e-=H2↑,则电池总反应式为Zn+2H+=H2↑+Zn2+,
(1)根据反电池总反应式计算Zn的质量;
(2)根据H原子守恒计算n(H2SO4),进而计算其物质的量浓度.
解答 解:该原电池中,锌电极上电极反应式为Zn-2e-=Zn2+,铜电极上电极反应式为2H++2e-=H2↑,则电池总反应式为Zn+2H+=H2↑+Zn2+,生成氢气的物质的量为:$\frac{3.36L}{22.4L/mol}$=0.15mol,
(1)由方程式可知,n(Zn)=n(H2)=0.15mol,故消耗Zn的质量为0.15mol×65g/mol=9.75g,故答案为:9.75g;
(2)根据氢原子守恒,得n(H2SO4)=n(H2)=0.15mol,则c(H2SO4)=$\frac{0.15}{0.2}$=0.75mol•L-1,故答案为:0.75mol•L-1.
点评 本题以原电池原理为载体,考查方程式的有关计算,题目难度不大,注意对基础知识的理解掌握.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:填空题
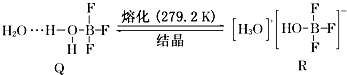
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铵和过氧化氢的分解 | B. | 二氧化硅与二氧化碳的熔化 | ||
| C. | 蔗糖和干冰的熔化 | D. | 氯化镁和氯化铝的熔化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
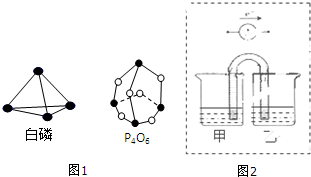
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取25g胆矾溶解在1L水中 | |
| B. | 将16g胆矾溶于水,然后将此溶液稀释至1L | |
| C. | 称取25g胆矾溶于水,然后将此溶液稀释至1L | |
| D. | 将胆矾加热除去结晶水后,称取16g溶解在1L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
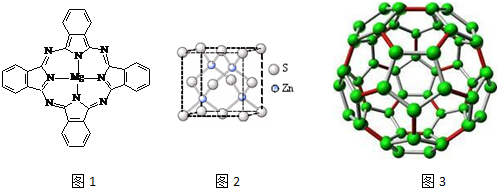
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴乙烷的消去反应:CH3CH2Br+NaOH$→_{△}^{H_{2}O}$CH2═CH2↑+NaBr+H2O | |
| B. | 苯酚钠溶液中通入CO2:2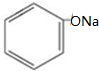 +CO2+H2O→2 +CO2+H2O→2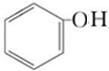 +Na2CO3 +Na2CO3 | |
| C. | 合成聚丙烯塑料:nCH2=CH-CH3$\stackrel{一定条件}{→}$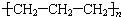 | |
| D. | 乙醛与新制银氨溶液反应:CH3CHO+2Ag(NH3)2OH$\stackrel{水溶液加热}{→}$CH3COONH4+2Ag↓+3NH3+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com