
���� ��Na2CO3���������Ʒ�Ӧ����NaOH��̼��ƣ�
��Na2CO3�������̼��ˮ��Ӧ����̼�����ƣ�
��ŨHNO3��ͭ��Ӧ����NO2��
��NH3����������һ��������
��ϡHNO3��ͭ��ӦNO��
��N2��������ӦNO��
��ŨH2SO4��ͭ�ڼ�������������SO2��
��CuO��ˮ����ӦCu��OH��2��
��NaHCO3���������Ʒ�Ӧ����Na2CO3��
��SO2��ˮ��Ӧ����H2SO3��
��1������ת���ж��ܷ�һ��ʵ�֣�
��2�������Ƿ��л��ϼ۱仯�ж��Ƿ���������ԭ��Ӧ����Ӧ���̴��ڻ��ϼ����ߣ�ʧȥ���ӵķ�Ӧ��Ҫ������������
��3������ת����ϵ�����ʵ�����д������ʽ��
��� �⣺��Na2CO3���������Ʒ�Ӧ����NaOH��̼��ƣ�Na2CO3��NaOH��һ��ʵ�֣�
��Na2CO3�������̼��ˮ��Ӧ����̼�����ƣ�Na2CO3��NaHCO3��һ��ʵ�֣�
��ŨHNO3��ͭ��Ӧ����NO2��HNO3��NO2��һ��ʵ�֣�
��NH3����������һ��������NH3��NO��һ��ʵ�֣�
��ϡHNO3��ͭ��ӦNO��HNO3��NO��һ��ʵ�֣�
��N2��������ӦNO��N2��NO2����һ��ʵ�֣�
��ŨH2SO4��ͭ�ڼ�������������SO2��H2SO4��SO2��һ��ʵ�֣�
��CuO��ˮ����ӦCu��OH��2��CuO��Cu��OH��2����һ��ʵ�֣�
��NaHCO3���������Ʒ�Ӧ����Na2CO3��NaHCO3��Na2CO3��һ��ʵ�֣�
��SO2��ˮ��Ӧ����H2SO3��SO2��H2SO3��һ��ʵ�֣�
��1��������ת���в���һ��ʵ�ֵ��ǣ��ޢࣻ
�ʴ�Ϊ�ޢࣻ
��2���ۢܢݢޢ��ж��л��ϼ۵ı仯������������ԭ��Ӧ��
��NH3��NO����N2��NO2��ת�������е�Ԫ�ػ��ϼ����ߣ�ʧȥ���ӣ���Ҫ������������
�ʴ𰸣��ۢܢݢޢߡ��ܢޣ�
��3������𰸲���Ψһ�ԣ�����������ֻ��һ���ο���ֻҪ����Ҫ������ԣ�
��Na2CO3�������̼��ˮ��Ӧ����̼�����ƣ����ӷ���ʽ��CO2+CO32-+H2O=2HCO3-��
�ʴ�Ϊ��CO2+CO32-+H2O=2HCO3-��
��ŨHNO3��ͭ��Ӧ����NO2�����ӷ���ʽ��Cu+4H++2NO3-=Cu2++2NO2��+2H2O��
�ʴ�Ϊ��Cu+4H++2NO3-=Cu2++2NO2��+2H2O��
�ܰ�������������һ��������ˮ����ѧ����ʽ��4NH3+5O2$\frac{\underline{\;����\;}}{��}$ 4NO+6H2O��
�ʴ�Ϊ��4NH3+5O2$\frac{\underline{\;����\;}}{��}$ 4NO+6H2O��
��ͭ��Ũ�����ڼ������������ɶ�����������ͭ��ˮ����ѧ����ʽ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�ʴ�Ϊ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
������ͭ�����ᷴӦ��������ͭ��ˮ������ͭ���������Ʒ�Ӧ����������ͭ�������ƣ�
��ѧ����ʽΪ��CuO+H2SO4=CuSO4+H2O��CuSO4+2NaOH=Cu��OH��2��+Na2SO4��
�ʴ�Ϊ��CuO+H2SO4=CuSO4+H2O��CuSO4+2NaOH=Cu��OH��2��+Na2SO4��
���� ���⿼�������ʵ�ת����������ԭ��Ӧ���жϡ����ӷ���ʽ����ѧ����ʽ��д����ȷ���ʵ������ǽ���ؼ�����Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 80g����狀��е�ԭ����ΪNA | |
| B�� | 1mol��������10NA������ | |
| C�� | 0.5ml��������ԭ����Ϊ0.5NA | |
| D�� | ��п��ϡ����ķ�Ӧ�У�1molпʧȥ�ĵ�����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

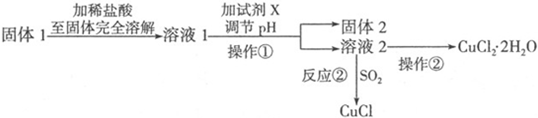
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
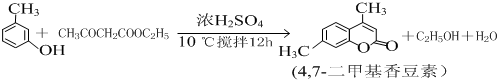
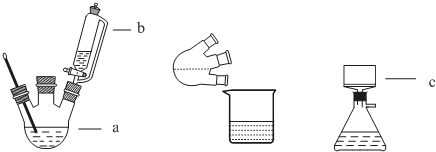
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | NO2 | B�� | NO | C�� | N2O | D�� | NH4NO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬŨ��ϡ��ҺpH��̼����ӣ����� | B�� | ���Ӱ뾶��O2-��F-��Na+��Mg2+ | ||
| C�� | �����۵㣺SiO2��P4��NaCl | D�� | �е㣺HF��HCl��HBr |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ļ�ѧ���ʻ��ã��������к� | |
| B�� | �����������뱵�ͬλ��ԭ�� | |
| C�� | �ԭ����7�����Ӳ㣬�������8������ | |
| D�� | ��ڳ����ǹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com