
【题目】为探究NaCl和CuSO4对唾液淀粉酶活性的影响,某同学进行了实验,实验步骤和结果见表.请回答:
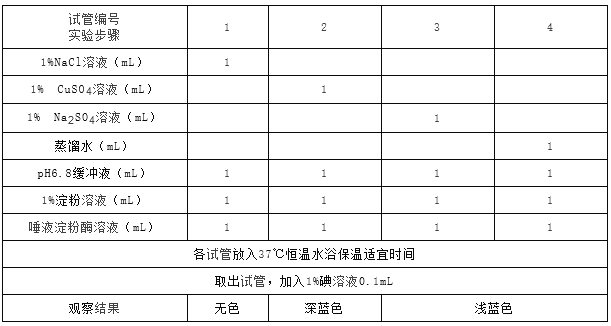
(1)实验中加入缓冲液的作用是 .
(2)分析实验结果可知:对酶活性有影响的离子是 ,其中对酶活性有抑制作用的离子是 ,对酶活性有促进作用的离子是 .
(3)该实验中设置4号试管的目的是 ;设置3号试管的目的是 .
(4)上述实验中若用斐林试剂代替碘溶液进行检测,1~4号试管中的颜色依次是 、 、 、 .根据上述实验结果,在操作过程中,保温之前不能加入斐林试剂,其原因是 .
【答案】(1)维持反应液中pH的稳定
(2)Cl﹣和Cu2+ Cu2+ C1﹣
(3)对照 确定Na+和SO42﹣对唾液淀粉酶的活性是否有影响
(4)深砖红色 无砖红色(或蓝色) 浅砖红色 浅砖红色 斐林试剂中有Cu2+,可抑制唾液淀粉酶的活性
【解析】
试题分析:分析实验结果:加入1% NaCl溶液的1号试管中,淀粉被淀粉酶水解了,可能是Na+或Cl﹣对酶的活性有促进作用,如果Na+能够促进唾液淀粉酶的活性,则3号试管中最后的结果应该也是无色,而3号试管中实验结果为浅蓝色,可见起促进作用的不是Na+,而是Cl﹣;同理,通过2号和3号试管的比较可知,Cu2+能够抑制唾液淀粉酶的活性.
解:(1)实验的自变量是加入的1% NaCl溶液、1% CuSO4、1% Na2SO4溶液和蒸馏水,为保证无关变量适宜且相同,实验中加入缓冲液的作用是维持反应液中pH的稳定.
(2)由以上分析可知,对酶活性有影响的离子是Cu2+、Cl﹣,其中对酶活性有抑制作用的离子是Cu2+,对酶活性有促进作用的离子是Cl﹣.
(3)该实验中,4号试管加入的是蒸馏水,其目的是作对照;3号试管加入的是1%Na2SO4溶液,其目的是排除1号试管中钠离子和2号试管中硫酸根离子对酶活性的影响.
(4)1号试管中的唾液淀粉酶的活性增强,淀粉被水解成葡萄糖,所以加入斐林试剂后有深砖红色沉淀生成;2号试管中的唾液淀粉酶的活性受抑制,淀粉未被水解成葡萄糖,所以加入斐林试剂后无砖红色沉淀生成:3号试管中的唾液淀粉酶的活性未受到影响,淀粉部分被水解成葡萄糖,所以加入斐林试剂后有浅砖红色沉淀生成;4号试管中的唾液淀粉酶的活性也未受到影响,结果同3号试管;斐林试剂中含有Cu2+,对淀粉酶的活性有影响,故保温之前不能加入斐林试剂.
故答案为:
(1)维持反应液中pH的稳定
(2)Cl﹣和Cu2+ Cu2+ C1﹣
(3)对照 确定Na+和SO42﹣对唾液淀粉酶的活性是否有影响
(4)深砖红色 无砖红色(或蓝色) 浅砖红色 浅砖红色 斐林试剂中有Cu2+,可抑制唾液淀粉酶的活性


 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料﹣﹣铁红(Fe2O3),具体生产流程如下:
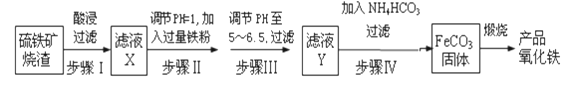
试回答下列问题:
(1)步骤Ⅰ若用稀硫酸,则Fe3O4发生反应的离子反应方程式为__________;
(2)实验室实现“步骤Ⅰ”中分离操作所用的玻璃仪器有__________________;步骤Ⅲ中应选用_____试剂调节溶液的pH(填字母编号).
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是_____________________;
(4)煅烧过程中发生反应的化学反应方程式为___________________;
(5)步骤Ⅳ中,FeCO3达到沉淀溶解平衡时,若室温下测得溶液的pH为9.5,c(Fe2+)=1×10﹣6 mol/L.试判断所得的FeCO3中是否含有Fe(OH)2,请通过简单计算说明理由_________________.(已知:Ksp[Fe(OH)2]=4.9×10﹣17).
(6)欲测定硫铁矿矿渣中Fe元素的质量分数,称取5.6 克样品,充分“酸溶”、“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体4.2克,测得该样品中Fe元素的质量分数为_______________(保留三位有效数字).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸产生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关乙烷、乙烯、乙炔分子结构的描述正确的是( )
A.这三种分子中均含有σ键和π键
B.这三种分子中的所有原子均处于同一平面上
C.碳碳键的键能:乙烯>乙炔>乙烷
D.碳碳键的键长:乙烷>乙烯>乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是人体某化学反应的图解,其中英文字母代表物质,数字表示反应前、中、后过程,有关叙述不正确的是( )
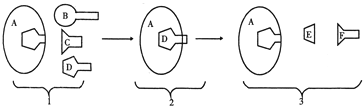
A. 图中代表酶的是A
B. 从图中1和2可以反映出酶具有专一性
C. 如果D代表脂肪,那么EF分别是甘油、脂肪酸
D. 酶之所以具有高效性是因为酶使反应活化能升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是
A. FeSO4具有氧化性,可用作食品抗氧化剂
B. SiO2熔点高、硬度大,可用于制光学仪器
C. Al(OH)3具有弱碱性,可用于制胃酸中和剂
D. NH3具有还原性,可用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系mA(g)+nB(g) ![]() pC(g)+qD(g) ΔH<0。下列结论中错误的是
pC(g)+qD(g) ΔH<0。下列结论中错误的是
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n
C.若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a
D.若温度不变压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com